题目内容
6.下列热化学方程式中,能够表示物质燃烧热的是( )| A. | C(s)+$\frac{1}{2}$O2(g)=CO(g)△H=-110.5 kJ/mol | |
| B. | H2(g)+Cl2(g)=2HCl(g)△H=-184.6 kJ/mol | |
| C. | H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H=-241.8 kJ/mol | |
| D. | C8H18(l)+$\frac{25}{2}$O2(g)=8CO2(g)+9H2O(l)△H=-5518 kJ/mol |
分析 在25℃,101 kPa时,1 mol可燃物完全燃烧生成稳定的化合物时所放出的热量,叫做该物质的燃烧热据此解答.
解答 解:A、根据燃烧热的含义,必须是1mol物质完全燃烧生成最稳定的产物放出的热量,应该是生成二氧化碳,不能是生成一氧化碳,故A错误;
B、燃烧热是指完全燃烧1mol物质生成稳定产物所放出的热量,该反应不是物质在氧气中的燃烧反应,故B错误;
C、根据燃烧热的含义,必须是1mol物质完全燃烧生成最稳定的产物放出的热量,该反应应该是生成液态水,不能是气态水,故C错误;
D、该热化学方程式符合燃烧热的含义:25℃,101 kPa时,1 mol庚烷完全燃烧生成稳定的化合物时所放出的热量,故D正确.
故选D.
点评 本题考查学生燃烧热的概念以及热化学方程式的书写知识,注意概念的理解和应用是解题的关键,难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
16.下列化学用语表示正确的是( )
| A. | CS2的比例模型: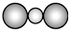 | |
| B. | H2O2的电子式: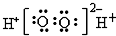 | |
| C. | 氯离子(Cl-)的结构示意图: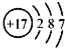 | |
| D. | 基态镁原子的电子排布图:1s22s22p63s2 |
17.下列事实不能用勒夏特列原理解释的是( )
| A. | 适当加热新制的氯水时,溶液的pH逐渐减小 | |
| B. | 加催化剂,使N2和H2在一定条件下转化为NH3 | |
| C. | 可用浓氨水和氢氧化钠固体快速制取氨气 | |
| D. | 增大压强,有利于SO2与O2反应生成SO3 |
11.等质量的下列物质分别完全燃烧,生成CO2的量最多的是( )
| A. | C2H6 | B. | C2H4 | C. | C2H2 | D. | C2H6O |
 (PAN)等二次污染物.
(PAN)等二次污染物.