题目内容
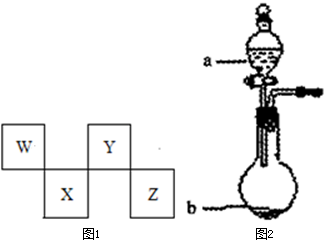
W、X、Y、Z四种短周期元素的原子序数X>W>Z>Y。W原子最外层电子数不超过最内层电子数。X原子L层电子数是其他各层电子总数的2倍。Y原子形成的气态氢化物分子与形成的最高价氧化物分子的电子数之比为5︰11。Z是自然界中含量最多的元素。(1)Y和Z形成的化合物与W和Z形成的化合物反应,其化学方程式可能是:________。
(2)Y元素可形成化学式为Y60的物质,该物质称为足球烯。已知该物质溶于苯等有机溶剂,熔点较低,由此可推测Y60晶体属于_______晶体,Y原子间形成_______键。
(3)W、X元素的最高价氧化物对应水化物的碱性强弱为________<________(用化学式表示)。
(4)这四种元素原子半径的大小为:________>________>________>________(填元素符号)。
答案:
解析:
解析:
| (1)Na2O2+CO2══Na2CO3 2Na2O2+2CO2══2Na2CO3+O2
(2)分子,非极性共价键 (3)Mg(OH)2<NaOH (4)Na>Mg>C>O (1)C60既为分子,显然为分子晶体,其与金刚石熔点孰高孰低,是很显然的。(2)既然C60中有30个C=C,则必可与30个F2加成。(3)由欧拉定律,可设单键为x,则:70+(12+20)-(30+x)=2。
|

练习册系列答案
 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案
相关题目
W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,其最外层电子数之和等于24,下列判断不正确的是( )
| W | X | |
| Y | Z |
| A、原子半径大小:W>X |
| B、元素最高正价:W>Z |
| C、简单阴离子的还原性:Y>Z |
| D、气态氢化物的稳定性:X>Y |
 W、X、Y、Z四种短周期元素在元素周期表中的位置如图所示,其中Z位于ⅦA族.请回答下列问题.
W、X、Y、Z四种短周期元素在元素周期表中的位置如图所示,其中Z位于ⅦA族.请回答下列问题.