题目内容
【题目】(1)利用反应![]() 设计成如图甲所示原电池,回答下列问题:
设计成如图甲所示原电池,回答下列问题:
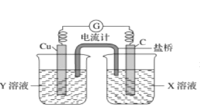
①写出电极反应式:正极________________。
②图中X溶液是_____,Y溶液是______。
③原电池工作时,盐桥中的___________(填“阳”或“阴”)离子向X溶液方向移动。
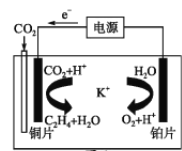
(2)利用一种钾盐水溶液作电解质,CO2电催化还原为乙烯,如图所示,在___(填“阳”或“阴”)极上产生乙烯的电极反应方程式为________。
【答案】Fe3+ + e- = Fe2+; FeCl3, CuCl2; 阳, 阴, 2CO2+ 12H+ + 12e- = C2H4 + 4H2O。
【解析】
本题考查电化学知识,原电池中,负极发生氧化反应,正极反生还原反应,溶液或盐桥中的阳离子向正极移动,阴离子向负极移动;电解池中与电源正极相连的是阳极,发生氧化反应,与电源负极相连的是阴极,发生还原反应。
(1)①C为正极,发生还原反应,电极方程式为2Fe3++2e-=2Fe2+,Cu为负极,电极方程式为Cu-2e-=Cu2+;
故答案是:Fe3+ +e- = Fe2+;
②铜被氧化,应为原电池负极,由装置图可知,Y是氯化铜溶液,电解质溶液X是FeCl3;
故答案是:X溶液是FeCl3,Y溶液是CuCl2;
③X是正极池,所以原电池工作时,盐桥中的阳离子向X溶液方向移动;
故答案为:阳;
(2)利用一种钾盐水溶液作电解质,CO2电催化还原为乙烯时,在阴极上产生乙烯的电极反应方程式为2CO2+ 12H+ + 12e- = C2H4 + 4H2O;
故答案是:阴;2CO2+ 12H+ + 12e- = C2H4 + 4H2O。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目