题目内容
6.Ⅰ.肼是一种高能燃料.已经各共价键键能(断裂或形成1mol共价键时吸收或释放的能量)如下:| N≡N | O=O | N-N | N-H | O-H | |
| 键能(KJ•mol-1) | 946 | 497 | 154 | 391 | 463 |
Ⅱ.密闭容器中进行反应:3Fe(s)+4H2O(g)?Fe3O4(s)+4H2(g)△H<02反应的化学平衡表达式为K=$\frac{{c}^{4}({H}_{2})}{{c}^{4}({H}_{2}O)}$.
(2)已知:600℃时,上述反应的平衡常数K=16.现有如图1甲(恒温恒压)和如图1乙(恒温恒容)两容器,起始时按下表所示分别加入各物质,体积为2L,在600℃时反应经过一段时间后均达平衡.
| Fe | H2O(g) | Fe3O4 | H2 | |
| 甲/mol | 2.0 | 1.0 | 2.0 | 0.5 |
| 乙/mol | 2.0 | 2.0 | 2.0 | 1.0 |

①关于甲、乙容器,下列说法正确的是AB
A.反应开始时两容器内的逆反应速率:甲<乙
B.若甲容器内气体的密度不再变化,则说明反应已达到平衡状态
C.若乙容器内气体的压强不再变化,则说明反应已达到平衡状态
D.平衡后添加Fe3O4 ,两容器内的平衡均逆向移动
②投料后甲5min达平衡,则此段时间内的平均反应速率v(H2)=0.05mol/(L•min-1)
③平衡后若将乙容器体系温度突然降低100℃,如图2下述图象中能正确反映平衡移动过程中容器内变化情况的是B.
3为恒容绝热容器,进行上述反应,起始与平衡时的各物质的量见下表:
| Fe | H2O(g) | Fe3O4 | H2 | |
| 起始/mol | 3.0 | 3.0 | 0 | 0 |
| 平衡/mol | m | n | p | q |
| Fe | H2O(g) | Fe3O4 | H2 | |
| A/mol | 3.0 | 3.0 | 0 | 0 |
| B/mol | 0 | 0 | 3.0 | 3.0 |
| C/mol | m | n | p | q |
分析 Ⅰ.(1)据热化学方程式的含义可知:旧键断裂所吸收的能量和新键生成所释放的能量之差即为化学反应焓变的数值,结合图示内容来回答即可;
Ⅱ.化学平衡表达式为K=$\frac{各个生成物平衡浓度系数次幂之积}{各个反应物平衡浓度系数次幂之积}$;
(2)①可逆反应达到平衡状态时,正逆反应速率相等(同种物质)或正逆反应速率之比等于系数之比(不同物质),平衡时各种物质的物质的量、浓度等不再发生变化,由此衍生的一些物理量不变;
②根据v=$\frac{△c}{△t}$进行计算;
③反应是放热反应,若将平衡体系温度降低100℃,平衡正向进行;容绝热根据反应时温度变化,判断平衡移动,分析氢气的百分含量,C条件下平衡不移动,A状况下,反应正向进行生成氢气,B状况下反应逆向进行生成Fe和水;
Ⅲ.根据氢氧化铁的Ksp=c(Fe3+)•c3(OH-)进行计算即可.
解答 解:Ⅰ.(1)根据图中内容,可以看出N2H4(g)+O2(g)?N2(g)+2H2O(l)反应的焓变等于旧键断裂吸收的能量和新键生成释放的能量之差,即△H=(154+391×4+497-946-463×4)kJ/mol=-583kJ/mol,故答案为:-583;
Ⅱ.化学平衡表达式为K=$\frac{各个生成物平衡浓度系数次幂之积}{各个反应物平衡浓度系数次幂之积}$=$\frac{{c}^{4}({H}_{2})}{{c}^{4}({H}_{2}O)}$;故答案为:$\frac{{c}^{4}({H}_{2})}{{c}^{4}({H}_{2}O)}$;
(2)①.A反应开始时两容器乙内的浓度较大,所以逆反应速率:甲<乙,故正确;
B.、水蒸气的密度与氢气的密度不同,所以当容器内的密度不变时,即是平衡状态,故正确;
C.该反应为气体体积不变的反应,所以容器内压强始终不变,不能用压强判断平衡状态,故错误;
D.平衡后添加Fe3O4,增加固体的量平衡不移动,故错误;
故选AB;
②投料后甲5min达平衡,则此段时间内的平均反应速率v(H2)=$\frac{△c}{△t}$=$\frac{\frac{0.5mol}{2L}}{5min}$=0.05mol/(L•min-1),故答案为:0.05mol/(L•min-1);
③反应是放热反应,若将平衡体系温度降低100℃,平衡正向进行;
A、逆向进行气体质量减小,故A不符合;
B、平衡正向进行,氢气物质的量增大,故B符合;
C、反应前后气体质量发生变化,密度随反应进行发生变化,故C不符合;
由于反应前后气体体积相等,所以C条件下,平衡不移动,氢气的体积分数与平衡是相同;A状况下,反应正向进行生成氢气,反应放出热量使容器温度升高,抑制反应继续生成氢气,故氢气体积分数较低,B状况下反应逆向进行生成Fe和水,是吸热过程,使容器温度降低,抑制反应继续消耗氢气,所以氢气的体积分数较高,故H2的百分含量按由大到小的顺序排列:B>C>A;
故答案为:B;B>C>A;
Ⅲ.根据氢氧化铁的Ksp=c(Fe3+)•c3(OH-),所以开始沉淀时,c((OH-)=$\root{3}{\frac{Ksp}{c(F{e}^{3+})}}$=$\root{3}{\frac{4×1{0}^{-38}}{0.04}}$=10-12mol/L,中和pH=1的盐酸,也会消耗氢氧化钠,所以消耗氢氧化钠的浓度是$\frac{0.1mol/L+1{0}^{-12}mol/L}{2}$≈0.05mol/L,故答案为:0.05.
点评 本题考查了化学平衡常数、盖斯定律、平衡状态的判断、Ksp的计算等,题目综合性较强,难度较大,侧重于对有关原理应用的考查.

 阅读快车系列答案
阅读快车系列答案| A. | 将0.1molK2SO4、0.1molNaCl、0.05molMgCl2溶于水制成100mL溶液 | |
| B. | 将0.05molK2SO4、0.1molNaCl、0.05molMgCl2溶于水制成100mL溶液 | |
| C. | 将0.1molK2SO4、0.05molNaCl、0.05molMgCl2溶于水制成100mL溶液 | |
| D. | 加入0.05molK2SO4、0.05molNaCl、0.1molMgCl2溶于水制成100mL溶液 |
| A. | 向氯化铝溶液中滴加少量氨水:Al3++3OH-═Al(OH)3↓+2H2O | |
| B. | 向氯化铁溶液中加入过量的锌粉:Zn+2Fe3+═2Fe2++Zn2+ | |
| C. | 以铁为电极电解NaCl溶液时,阳极的电极反应:Fe-3e-═Fe3+ | |
| D. | 硝酸亚铁溶液中滴入浓盐酸:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O |
| A. | 1g碳燃烧生成一氧化碳时放出126.4kJ的热量 | |
| B. | 1mol固体碳在氧气中燃烧生成一氧化碳气体时放出126.4kJ的热量 | |
| C. | 12g碳燃烧生成一氧化碳时吸收126.4kJ的热量 | |
| D. | 碳的燃烧热为126.4kJ/mol |
 某温度下,溶液中c(H+)=10xmol•L-1,c(OH-)=10ymol•L-1,x和y的关系如图所示.则该温度下,0.01mol•L-1的NaOH溶液的pH为( )
某温度下,溶液中c(H+)=10xmol•L-1,c(OH-)=10ymol•L-1,x和y的关系如图所示.则该温度下,0.01mol•L-1的NaOH溶液的pH为( )| A. | 10 | B. | 11 | C. | 13 | D. | 12 |
| A. | 将①、④等体积混合,混合液一定呈碱性 | |
| B. | 将②、③混合,若有pH=7,则消耗溶液的体积:②=③ | |
| C. | 水的电离程度:①<② | |
| D. | 将四份溶液稀释相同倍数后,溶液的pH:③>④,②>① |
| A. | 反应物A或B至少有一个是气体 | B. | 容器内不可能是单一气体 | ||
| C. | m+n可能大于p+q | D. | 若m<p,且D是气体,则B一定是气体 |
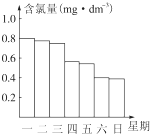 某校高一化学研究性学习小组对日常生活中的氯气用途进行了调查,了解到氯气可广泛地应用于衣物的漂白、水体的杀菌和消毒等.
某校高一化学研究性学习小组对日常生活中的氯气用途进行了调查,了解到氯气可广泛地应用于衣物的漂白、水体的杀菌和消毒等.