题目内容
水是一种重要的自然资源,是人类赖以生存不可缺少的物质.水质优劣直接影响人体健康.请回答下列问题:(1)天然水中溶解的气体主要有 、 .
(2)天然水在净化处理过程中加入的混凝剂可以是 其纯净水作用的原理是
(3)水的纯净和软化的区别是
(4)硬度为1°的水是指每升水含10mgCaO或与之相当的物质(如7.1mgMgO).若某天然水中c(Ca2+)=1.2×10-3mol?L-1,c(Mg2+)=6×10-4mol?L-1,则此水的硬度为 ;
(5)若(4)中的天然水还含有c(HCO3-1)=8×10-4mol?L-1,现要软化10m3这种天然水,则需先加入Ca(OH)2 g,后加入Na2CO3 g.
【答案】分析:(1)空气中的氧气不易溶于水,二氧化碳能溶于水,其它气体一般是难溶于水;
(2)混凝剂是溶液中水解生成胶体的盐类,净水作用是吸附悬浮杂质使其聚沉达到净化目的;
(3)净化水是除去悬浮杂质,软化水是除去钙镁离子;
(4)依据硬度为1°的水是指每升水含10mgCaO或与之相当的物质(如7.1mgMgO),将水中的Ca2+、Mg2+质量折算成CaO的质量计算得到;
(5)硬水软化需要把钙离子和镁离子全部沉淀,加入氢氧化钙和镁离子、碳酸氢根离子反应,加入碳酸钠沉淀钙离子.
解答:解:(1)氧气能够较少量地溶解在水中,二氧化碳能够较多量地溶解在水中,所以天然水中溶解的气体主要有氧气和二氧化碳,故答案为:O2;CO2(或氮气);
(2)混凝剂是吸附水中的微小悬浮颗粒,凝聚成较大的颗粒,而快速沉降的主要作用,要具备水解生成胶体的性质,所以常有铝盐或铁盐在水中发生水解生成相应氢氧化物胶体,如明矾、硫酸铝、硫酸铁、硫酸亚铁等,
故答案为:明矾、硫酸铝、硫酸铁、硫酸亚铁;铝盐或铁盐在水中发生水解生成相应氢氧化物胶体,它可吸附天然水中悬浮物并破坏天然水中的其他带异电的胶体,使其聚沉,达到净化目的;
(3)水的净化是除去悬浮性杂质,一般用明矾进行;水的软化是降低Ca2+、Mg2+的浓度,方法很多,有离子交换法、石灰纯碱法等,
故答案为:水的净化是用混凝剂(如明矾等)将水中胶体及悬浮物沉淀下来,而水的软化是除去水中的钙离子和镁离子;
(4)某天然水中c(Ca2+)=1.2×10-3mol?L-1,c(Mg2+)=6×10-4mol?L-1,硬度为1°的水是指每升水含10mgCaO或与之相当的物质(如7.1mgMgO);1L水中钙离子物质的量=1.2×10-3mol,相当于CaO质量=1.2×10-3mol×56g/mol=67.2mg,1L水中镁离子物质的量=6×10-4mol,相当于氧化镁质量6×10-4mol×40g/mol=24mg,所以水的硬度=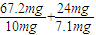 =10°故答案为:10°;
=10°故答案为:10°;
(5)10m3这种天然水水中含有钙离子物质的量=10×103L×1.2×10-3mol?L-1=12mol;镁离子物质的量=10×103L×6×10-4mol?L-1=6mol;碳酸氢根离子物质的量=10×103L×8×10-4mol?L-1=8mol;加入氢氧化钙发生的反应为:
Mg2++2OH-=Mg(OH)2↓ HCO3-+OH-=CO32-+H2O
1 2 1 1 1
6mol 12mol 8mol 8mol 8mol
共需氢氧根物质的量20mol;
需要Ca(OH)2物质的量10mol,氢氧化钙质量为74g/mol×10mol=740g,
水溶液中Ca2+物质的量为12mol+10mol=22mol,
其中需要加入的 碳酸根离子为22mol-8mol=14mol,需要碳酸钠的质量为14mol×106g/mol=1484g,
故答案为:740;1484.
点评:本题考查了盐类水解的应用,净水方法和软化原理,水的硬度计算需要理解题干信息,准确计算,题目难度中等.
(2)混凝剂是溶液中水解生成胶体的盐类,净水作用是吸附悬浮杂质使其聚沉达到净化目的;
(3)净化水是除去悬浮杂质,软化水是除去钙镁离子;
(4)依据硬度为1°的水是指每升水含10mgCaO或与之相当的物质(如7.1mgMgO),将水中的Ca2+、Mg2+质量折算成CaO的质量计算得到;
(5)硬水软化需要把钙离子和镁离子全部沉淀,加入氢氧化钙和镁离子、碳酸氢根离子反应,加入碳酸钠沉淀钙离子.
解答:解:(1)氧气能够较少量地溶解在水中,二氧化碳能够较多量地溶解在水中,所以天然水中溶解的气体主要有氧气和二氧化碳,故答案为:O2;CO2(或氮气);
(2)混凝剂是吸附水中的微小悬浮颗粒,凝聚成较大的颗粒,而快速沉降的主要作用,要具备水解生成胶体的性质,所以常有铝盐或铁盐在水中发生水解生成相应氢氧化物胶体,如明矾、硫酸铝、硫酸铁、硫酸亚铁等,
故答案为:明矾、硫酸铝、硫酸铁、硫酸亚铁;铝盐或铁盐在水中发生水解生成相应氢氧化物胶体,它可吸附天然水中悬浮物并破坏天然水中的其他带异电的胶体,使其聚沉,达到净化目的;
(3)水的净化是除去悬浮性杂质,一般用明矾进行;水的软化是降低Ca2+、Mg2+的浓度,方法很多,有离子交换法、石灰纯碱法等,
故答案为:水的净化是用混凝剂(如明矾等)将水中胶体及悬浮物沉淀下来,而水的软化是除去水中的钙离子和镁离子;
(4)某天然水中c(Ca2+)=1.2×10-3mol?L-1,c(Mg2+)=6×10-4mol?L-1,硬度为1°的水是指每升水含10mgCaO或与之相当的物质(如7.1mgMgO);1L水中钙离子物质的量=1.2×10-3mol,相当于CaO质量=1.2×10-3mol×56g/mol=67.2mg,1L水中镁离子物质的量=6×10-4mol,相当于氧化镁质量6×10-4mol×40g/mol=24mg,所以水的硬度=
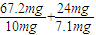 =10°故答案为:10°;
=10°故答案为:10°;(5)10m3这种天然水水中含有钙离子物质的量=10×103L×1.2×10-3mol?L-1=12mol;镁离子物质的量=10×103L×6×10-4mol?L-1=6mol;碳酸氢根离子物质的量=10×103L×8×10-4mol?L-1=8mol;加入氢氧化钙发生的反应为:
Mg2++2OH-=Mg(OH)2↓ HCO3-+OH-=CO32-+H2O
1 2 1 1 1
6mol 12mol 8mol 8mol 8mol
共需氢氧根物质的量20mol;
需要Ca(OH)2物质的量10mol,氢氧化钙质量为74g/mol×10mol=740g,
水溶液中Ca2+物质的量为12mol+10mol=22mol,
其中需要加入的 碳酸根离子为22mol-8mol=14mol,需要碳酸钠的质量为14mol×106g/mol=1484g,
故答案为:740;1484.
点评:本题考查了盐类水解的应用,净水方法和软化原理,水的硬度计算需要理解题干信息,准确计算,题目难度中等.

练习册系列答案
相关题目