题目内容
某白色固体易溶于水,将所得无色溶液分成两部分,取一部分加过量的NaOH溶液并微热,产生一种使湿润的红色石蕊试纸变蓝色的气体,另一部分加入氯水振荡后,溶液呈棕黄色.则原固体是( )
| A、NH4NO3 | B、NaBr | C、NH4I | D、(NH4)2CO3 |
分析:根据加过量的NaOH溶液并微热,产生一种使湿润的红色石蕊试纸变蓝色的气体,可以判断白色固体中一定含有铵离子;根据加入氯水振荡后,溶液呈棕黄色,可以判断固体中一定含有碘离子,据此完成本题.
解答:解:取一部分加过量的NaOH溶液并微热,产生一种使湿润的红色石蕊试纸变蓝色的气体,该气体为氨气,证明原白色固体中一定含有铵离子;
另一部分加入氯水振荡后,溶液呈棕黄色,棕黄色的为碘单质溶液,说明白色固体中含有碘离子,
根据以上分析可知,该白色固体为NH4I,
故选C.
另一部分加入氯水振荡后,溶液呈棕黄色,棕黄色的为碘单质溶液,说明白色固体中含有碘离子,
根据以上分析可知,该白色固体为NH4I,
故选C.
点评:本题考查物质的检验与鉴别,该题是高考中的常见题型,属于中等难度的试题,试题综合性强,有利于培养学生的逻辑思维能力和发散思维能力,提高学生的应试能力和学习效率.该类试题需要注意的是进行物质的检验时,要依据物质的特殊性质和特征反应,选择适当的试剂和方法,准确观察反应中的明显现象,如颜色的变化、沉淀的生成和溶解、气体的产生和气味、火焰的颜色等,进行判断、推理、验证即可.

练习册系列答案
相关题目
某混合金属粉末,除Mg外,还含有Al、Zn中的一种或两种,含量都在10%以上.某研究小组设计实验探究该混合金属粉末中铝、锌元素的存在.
所用试剂:样品、pH试纸、稀H2SO4、NaOH溶液、稀NH3·H2O.
该小组探究过程如下:
●查阅资料:
|
①镁、铝、锌都是银白色的金属; ②锌(Zn)可以与NaOH溶液反应生成H2; ③Zn(OH)2为白色固体,难溶于水,可溶于强碱及NH3·H2O; ④Zn2+易形成络合物如[Zn(NH3)4]2+,该络合物遇强酸分解生成Zn2+、NH4+. |
● 提出假设:
(1)假设①:该混合金属粉末中除镁外还含有________元素
假设②:该混合金属粉末中除镁外还含有________元素
假设③:该混合金属粉末中除镁外还含有铝、锌元素
●实验探究:
甲同学基于假设③设计实验方案如下:
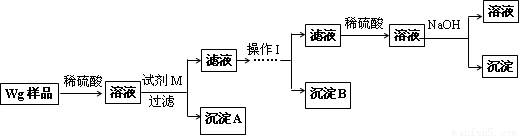
乙同学同样基于假设3设计另一实验方案如下:
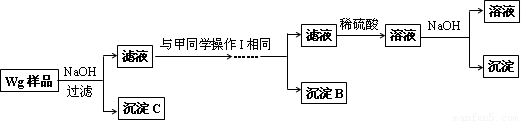
(2)试剂M是____________,沉淀B是_____________.
(2)试剂M是____________,沉淀B是_____________.
(3)丙同学认为乙同学的方案比甲同学的好,理由是_______________________.
(4)丁同学研究了甲、乙两同学的方案后,在其中一种方案的基础上用最简便方法测定了Wg样品中金属镁(Mg)的质量,他的方法是____________________________.
(5)操作Ⅰ的主要过程是:在滤液中逐滴加入_______________,直至生成的沉淀刚好溶解,再加入足量的____________________.


