��Ŀ����
��ɫ����ۺ���������SPFS����һ����Ҫ�����߷�������������������ˮ����Ϊ��ҵ��������ˮ���������������Ҫ��Ӧ�ã�SPFS�ɱ�ʾ��Fex��OH��y��SO4��z?nH2O����ҵ�ϳ��õ�һ���Ʊ�����Ϊ��
��SPFS�Ķ������ָ���У��λ�������Ҫ������ָ��֮һ���λ��ȶ���Ϊ��
���=
��100%��ʽ��n��OH-����n��Fe���ֱ��ʾ����ۺ���������OH-��Fe�����ʵ�����
�Իش��������⣮
��1��ȡ7.51gij����ۺ��������ܽ���ˮ�������м��������BaCl2��Һ��������ȫ�������ˡ�ϴ�ӡ�����ð�ɫ����10.48g����������Һ�м���NH3?H2O��������ҺpH=6�������ˡ�ϴ�ӡ������Fe2O3����2.80g���ù���ۺ����������λ���Ϊ
��2���ù���ۺ���������Ʒ�Ļ�ѧʽΪ

��SPFS�Ķ������ָ���У��λ�������Ҫ������ָ��֮һ���λ��ȶ���Ϊ��
���=
| n(OH-) | 3n(Fe) |
�Իش��������⣮
��1��ȡ7.51gij����ۺ��������ܽ���ˮ�������м��������BaCl2��Һ��������ȫ�������ˡ�ϴ�ӡ�����ð�ɫ����10.48g����������Һ�м���NH3?H2O��������ҺpH=6�������ˡ�ϴ�ӡ������Fe2O3����2.80g���ù���ۺ����������λ���Ϊ
14.29%
14.29%
����2���ù���ۺ���������Ʒ�Ļ�ѧʽΪ
Fe35��OH��15��SO4��45?54H2O
Fe35��OH��15��SO4��45?54H2O
����������1��������Ԫ�ء���������ӵ��غ��ϵ��ȷ������������֪��Ϣ�����λ��ȣ�
��2������ԭ���غ�������غ������㣮
��2������ԭ���غ�������غ������㣮
����⣺��1�����������������������Լ���ã�n��Fe��=
mol��2=0.035mol��ȡ7.51gij����ۺ��������ܽ���ˮ�������м��������BaCl2��Һ��������ȫ�������ˡ�ϴ�ӡ�����ð�ɫ����10.48g����Ϊ���ᱵ������������10.48g��
����n��SO42-��=
=0.045mol������n��OH-��=3��n��Fe��-2��n��SO42-��=3��0.035-2��0.045=0.015mol��
�����=
��100%=
��100%=14.29%��
�ʴ�Ϊ��14.29%��
��2�����������غ���Եó�Fex��OH��y��SO4��z?nH2O��ˮ����n��H2O��=��7.51g-0.035mol��56g?mol-1-0.045mol��96 g?mol-1-0.015mol��17 g?mol-1��/18 g?mol-1=0.054mol����֪����n��Fe��=0.035mol��n��OH-��=0.015mol��n��SO42-��=0.045mol��
��ѧʽ�и�Ԫ�ص����ʵ���֮�ȵ��������ֵ�ȣ�����ѧʽ��Fe35��OH��15��SO4��45?54H2O��
�ʴ�Ϊ��Fe35��OH��15��SO4��45?54H2O��
| 2.8 |
| 160 |
����n��SO42-��=
| 10.48g |
| 233g/mol |
�����=
| n(OH-) |
| 3n(Fe) |
| 0.015mol |
| 3��0.035mol |
�ʴ�Ϊ��14.29%��
��2�����������غ���Եó�Fex��OH��y��SO4��z?nH2O��ˮ����n��H2O��=��7.51g-0.035mol��56g?mol-1-0.045mol��96 g?mol-1-0.015mol��17 g?mol-1��/18 g?mol-1=0.054mol����֪����n��Fe��=0.035mol��n��OH-��=0.015mol��n��SO42-��=0.045mol��
��ѧʽ�и�Ԫ�ص����ʵ���֮�ȵ��������ֵ�ȣ�����ѧʽ��Fe35��OH��15��SO4��45?54H2O��
�ʴ�Ϊ��Fe35��OH��15��SO4��45?54H2O��
����������̽���˹���ۺ���������Ʒ����ɣ���һ������֪ʶ����Ŀ������ѧ�������ͽ��������������ۺ��Խ�ǿ�������Ѷ��Դ�

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ


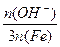 �� 100% ��ʽ��n(OH-)��n(Fe)�ֱ��ʾ����ۺ���������OH����FeԪ�ص����ʵ�������ش��������⣺
�� 100% ��ʽ��n(OH-)��n(Fe)�ֱ��ʾ����ۺ���������OH����FeԪ�ص����ʵ�������ش��������⣺
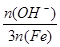 �� 100% ��ʽ��n(OH-)��n(Fe)�ֱ��ʾ����ۺ���������OH����FeԪ�ص����ʵ�������ش��������⣺
�� 100% ��ʽ��n(OH-)��n(Fe)�ֱ��ʾ����ۺ���������OH����FeԪ�ص����ʵ�������ش��������⣺