题目内容
18.下列关于有机化合物的说法正确的是( )| A. | 能发生银镜反应的有机物一定属于醛类 | |
| B. | 乙烯和聚乙烯互为同系物 | |
| C. | 室温下,乙醇在水中的溶解度大于溴乙烷 | |
| D. | 乙醇与乙醚互为同分异构体 |
分析 A.葡萄糖、醛、甲酸以及甲酸酯都可发生银镜反应;
B.乙烯和聚乙烯的结构不同;
C.乙醇分子间存在氢键;
D.乙醇和乙醚的分子式不同.
解答 解:A.发生银镜反应的有机物含有醛基,但含有醛基的不一定为醛类,如葡萄糖、醛、甲酸以及甲酸酯等,故A错误;
B.乙烯含有碳碳双键,聚乙烯为乙烯的加聚产物,二者结构不同,不是同系物,故B错误;
C.乙醇分子间存在氢键,易溶于水,故C正确;
D.乙醇和乙醚的分子式不同,二者不是同分异构体,故D错误.
故选C.
点评 本题考查有机物的 结构与性质,为高频考点,把握官能团与性质的关系、有机反应为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
9.下列物质中,属于天然有机高分子化合物的是( )
| A. | 蚕丝 | B. | 塑料 | C. | 化学纤维 | D. | 合成橡胶 |
9.已知  ,下列说法错误的是( )
,下列说法错误的是( )
 ,下列说法错误的是( )
,下列说法错误的是( )| A. | M的分子式为C7H12 | |
| B. | N中所有的碳原子不可能在同一平面 | |
| C. | M可以发生取代反应和加成反应 | |
| D. | 比N少一个碳原子且为N的同系物的同分异构体有22种 |
6.在容积不变的密闭容器中,发生反应CO(g)+2H2(g)?CH3OH(g),充入1mol CO和2mol H2后,下列说法能判断达到化学平衡状态的是( )
| A. | H2的消耗速率等于CH3OH的生成速率的2倍 | |
| B. | CO和H2的转化率相等 | |
| C. | 容器内的压强不再改变 | |
| D. | 体系中气体的密度不再改变 |
5.一定条件下,向某容积可变的密闭容器中充入2mol SO2和1mol O2发生反应:2SO2+O2?2SO3.下列说法不正确的是( )
| A. | 升高温度能加快化学反应速率 | B. | 减小压强能减慢化学反应速率 | ||
| C. | 反应生成SO3的物质的量小于2 mol | D. | 达平衡时反应即停止 |
12.化学实验如果设计或操作不当,可能看不到预期的现象.下列关于实验现象的分析不正确的是( )
| 选项 | A | B | C | D |
| 装置 |  甲烷与氯气反应 |  苯酚与溴水反应 |  银镜反应 |  制备乙酸乙酯 |
| 现象 | 量筒中未出现油状液体 | 试管中未看到白色沉淀 | 试管中有黑色沉淀,但未出现银镜 | NaOH溶液中未看到油状液体 |
| 原因 | 甲烷与氯气未反应 | 苯酚浓度较大 | 反应未生成单质银 | 产物水解 |
| A. | A | B. | B | C. | C | D. | D |
9.已知反应2I-+S2O82-═I2+2SO42-,加入淀粉溶液可观察到溶液变蓝色.反应速率可以用淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大.20℃时得到如下实验数据:
分析上述数据,下列说法正确的是( )
| 实验编号 | C(I-)/mol•L | C(S2O82-)/mol•L | t/s |
| 1 | 0.040 | 0.040 | 88.0 |
| 2 | 0.080 | 0.040 | 44.0 |
| 3 | 0.080 | 0.080 | 22.0 |
| 4 | 0.160 | 0.020 | 44.0 |
| 5 | 0.120 | 0.040 | 29.3 |
| A. | I-的浓度越大,反应速率越快 | |
| B. | S2O82- 的浓度越大,反应速率越快 | |
| C. | 该实验的目的是研究 I- 与S2O82- 的浓度对反应速率的影响 | |
| D. | 5个实验中,编号3对应浓度的实验,反应速率最慢 |
14.25℃时,下列指定溶液中微粒的物质的量浓度关系正确的是( )
| A. | 0.1mol•L-1Na2S溶液中:c(OH-)=c(H2S)+c(HS-) | |
| B. | 0.1mol•L-1 CH3COONH4溶液中:c(NH4+)+c(NH3•H2O)=c(CH3COO-)+c(CH3COOH) | |
| C. | 0.1mol•L-1pH=6的NaHSO3溶液中:c(Na+)>c(HSO3-)>c(SO32-)>c(H2SO3) | |
| D. | 0.1mol•L-1Na2CO3溶液与0.1mol•L-1NaHCO3溶液等体积混合所得溶液中:c(CO32-)>c(HCO3-)>c(OH-)>c(H2CO3) |
 、乙:HOOH,式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂.化学家Baeyer和Villiyer为研究H2O2的结构,设计并完成了下列实验:a.将C2H5OH与浓H2SO4反应生成(C2H5)2SO4和水;b.将制得的(C2H5)2SO4与H2O2反应,只生成A和H2SO4;c.将生成的A与H2反应(已知该反应中H2做还原剂).
、乙:HOOH,式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂.化学家Baeyer和Villiyer为研究H2O2的结构,设计并完成了下列实验:a.将C2H5OH与浓H2SO4反应生成(C2H5)2SO4和水;b.将制得的(C2H5)2SO4与H2O2反应,只生成A和H2SO4;c.将生成的A与H2反应(已知该反应中H2做还原剂).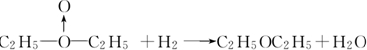 .
.