题目内容
某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(图中p表示压强,T表示温度,n表示物质的量):

根据以上规律判断,下列结论正确的是
- A.反应Ⅰ:ΔH>0,p2>p1
- B.反应Ⅱ:ΔH<0,T1>T2
- C.反应Ⅲ:ΔH>0,T2>T1或ΔH<0,T2<T1
- D.反应Ⅳ:ΔH<0,T2>T1
BC
反应Ⅰ的特点是正反应方向为气体减小的方向结合图像,压强增大A的转化率应增大,所以P2>P1,它随温度的升高A的转化率降低,所以正反应为放热反应ΔH<0,故A错。关于反应Ⅱ由图像可以看出T1条件下达到平衡所用时间少所以T1>T2,而在T1条件下达平衡时n(C)小,所以说明低温有利于C的生成,故它主要的正反应为放热反应ΔH<0,B正确;关于反应Ⅲ,由图像可以看出,T2条件下C的平衡体积分数大,因此当T2>T1时正反应应为吸热反应ΔH>0,而当T2<T1时,正反应应为放热反应ΔH<0,故C正确;关于反应Ⅳ,由图像可以看出T2条件下A的转化率大,因此当T2>T1时,说明升高温度平衡向正反应方向进行,因此正反应为吸热反应ΔH<0,所以D错。
反应Ⅰ的特点是正反应方向为气体减小的方向结合图像,压强增大A的转化率应增大,所以P2>P1,它随温度的升高A的转化率降低,所以正反应为放热反应ΔH<0,故A错。关于反应Ⅱ由图像可以看出T1条件下达到平衡所用时间少所以T1>T2,而在T1条件下达平衡时n(C)小,所以说明低温有利于C的生成,故它主要的正反应为放热反应ΔH<0,B正确;关于反应Ⅲ,由图像可以看出,T2条件下C的平衡体积分数大,因此当T2>T1时正反应应为吸热反应ΔH>0,而当T2<T1时,正反应应为放热反应ΔH<0,故C正确;关于反应Ⅳ,由图像可以看出T2条件下A的转化率大,因此当T2>T1时,说明升高温度平衡向正反应方向进行,因此正反应为吸热反应ΔH<0,所以D错。

练习册系列答案
 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
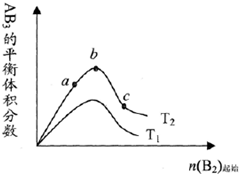 某化学科研小组研究在其他条件不变时,改变某一条件对A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度)由此可得出的结论是( )
某化学科研小组研究在其他条件不变时,改变某一条件对A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度)由此可得出的结论是( )| A、反应速率a>b>c | B、达到平衡时A2的转化率大小为:b>a>c | C、若T2>T1,则正反应一定是吸热反应 | D、达到平衡时,AB3的物质的量大小为:c>b>a |
某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(图中P表示压强,T表示温度,n表示物质的量):

根据以上规律判断,下列结论正确的是( )

根据以上规律判断,下列结论正确的是( )
| A、反应Ⅰ:△H>0,P2>P1 | B、反应Ⅱ:△H<0,T1<T2 | C、反应Ⅲ:△H>0,T2>T1或△H<0,T2<T1 | D、反应Ⅳ:△H<0,T2>T1 |
 (2009?浙江模拟)某化学科研小组研究在其他条件不变时,改变某一条件对A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量),根据右图可得出的判断结论正确的是( )
(2009?浙江模拟)某化学科研小组研究在其他条件不变时,改变某一条件对A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量),根据右图可得出的判断结论正确的是( ) 某化学科研小组研究在其他条件不变时,改变某一条件对A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如下图所示的变化规律(图中T表示温度,n表示物质的量),根据如图可得出的判断结论正确的是( )
某化学科研小组研究在其他条件不变时,改变某一条件对A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如下图所示的变化规律(图中T表示温度,n表示物质的量),根据如图可得出的判断结论正确的是( ) 某化学科研小组研究在其它条件不变时,改变某一条件对A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响时,得到如图所示的变化规律(图中T表示温度,n表示物质的量),根据图示得出的结论中正确的是( )
某化学科研小组研究在其它条件不变时,改变某一条件对A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响时,得到如图所示的变化规律(图中T表示温度,n表示物质的量),根据图示得出的结论中正确的是( )