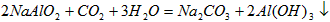题目内容
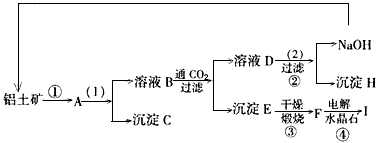
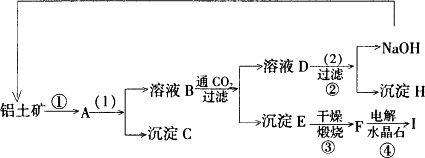
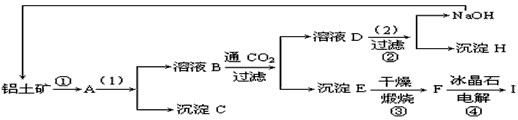
工业制备铝一般是从铝土矿(主要成分是Al2O3,含有Fe2O3杂质)中得到纯净的是Al2O3,然后电解是Al2O3得到铝。下图是从铝土矿中提纯是Al2O3的简单示意图。其中牵涉到的一个反应是:2NaAlO2+CO2+3H2O=Na2CO3+2Al(OH)3↓。
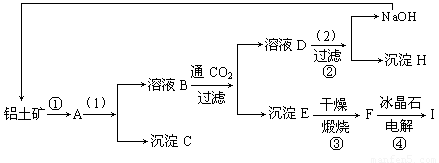
(1)写出图示中(1)的实验操作是 ;图示中(2)加入的试剂 。
(2)试推断物质(写化学式)B ;C ;H ;F 。
(3)写出化学方程式:
① 。
② 。
③ 。
④ 。
(1)过滤;Ca(OH)2;(2)NaAlO2;Fe2O3;CaCO3;Al2O3;
(3)① Al2O3+2NaOH=2NaAlO2+H2O ②Na2CO3+Ca(OH)2=CaCO3↓+ 2NaOH
③2Al(OH)3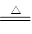 Al2O3+3H2O ④2Al2O3
Al2O3+3H2O ④2Al2O3 4Al+3O2↑
4Al+3O2↑
【解析】
试题分析:(1)将沉淀从溶液中分离出来的操作是过滤;根据反应2NaAlO2+CO2+3H2O=Na2CO3+2Al(OH)3↓可知,D中含有碳酸钠,E是氢氧化铝,则F是氧化铝,电解氧化铝即得到金属铝。碳酸钠要生成氢氧化钠和沉淀,需要进入的试剂是氢氧化钙,即(2)中加入的试剂是氢氧化钙。
(2)B中通入CO2即生成氢氧化铝沉淀,说明B中含有偏铝酸钠,所以反应①加入的试剂是氢氧化钠,则C是氧化铁。根据(1)中的分析可知,H是碳酸钙,F是氧化铝。
(3)反应①是氧化铝和氢氧化钠溶液的反应,化学方程式是Al2O3+2NaOH=2NaAlO2+H2O;反应②是碳酸钠和氢氧化钙的反应,化学方程式是Na2CO3+Ca(OH)2=CaCO3↓+ 2NaOH;反应③是氢氧化铝的分解反应,化学方程式是2Al(OH)3 Al2O3+3H2O;反应④是电解熔融的氧化铝,化学方程式是2Al2O3
Al2O3+3H2O;反应④是电解熔融的氧化铝,化学方程式是2Al2O3 4Al+3O2↑。
4Al+3O2↑。
考点:考查金属铝的冶炼、物质的分离和提纯、化学实验基本操作、试剂的选择和方程式的书写。
点评:该题是高考中的常见题型,属于中等难度的试题试题基础性强,难易适中,注重考查学生灵活运用基础知识解决实际问题的能力。本题要求学生必须认真、细致的审题,联系所学过的知识和技能,进行知识的类比、迁移、重组,全面细致的思考才能得出正确的结论。



 CO↑+H2O 请根据以下各装置进行选择组成一套相对较为合理的实验装置图(某些装置可重复使用)
CO↑+H2O 请根据以下各装置进行选择组成一套相对较为合理的实验装置图(某些装置可重复使用)