题目内容
【题目】下列实验操作会引起实验结果偏高的是( )
A.测定硫酸铜晶体中结晶水含量的实验中,晶体加热完全失去结晶水后,将盛试样的坩埚放在实验桌上自行冷却
B.镀锌铁皮锌镀层厚度测量实验中,将铁皮用酒精灯持续加强热以彻底烘干
C.用标准碱滴定待测酸溶液时,装有标准碱的滴定管滴定前无气泡,滴定后有气泡
D.一定物质的量浓度的盐酸配制过程中用量筒量取计算所需的浓盐酸时,仰视观察刻度线
【答案】D
【解析】
A. 在硫酸铜晶体(CuSO4nH2O)结晶水含量测定中,加热前后质量的减少量即是失去结晶水的质量,加热后放在空气中冷却,会吸收空气中的水重新形成晶体,反应前后质量差减小,结果偏小,故A错误;
B. 镀锌铁皮锌镀层厚度测量实验中,将铁皮用酒精灯持续加强热以彻底烘干,加热时铁粉能被氧化,导致质量差偏小,根据测量原理厚度 ,可知,测定结果偏低,故B错误;
,可知,测定结果偏低,故B错误;
C. 用标准碱滴定待测酸溶液时,装有标准碱的滴定管滴定前无气泡,滴定后有气泡,则标准液的体积偏小,即标准液物质的量偏小,导致待测液浓度偏低,C错误;
D. 一定浓度的盐酸配制过程中,用量筒量取计算所需的浓盐酸时,仰视观察刻度线,会导致量取液体的体积偏大,溶质变多,所配溶液浓度偏高,故D正确;
答案选D。

【题目】(NH4)2Fe(SO4)2·6H2O俗称摩尔盐(M=392g·mol-1)是分析化学中重要的标准物质,某研究小组拟采用硫铁矿焙烧后的烧渣(主要成分为Fe2O3、SiO2、Al2O3,不考虑其他杂质)为原料制取摩尔盐,设计了如下流程:
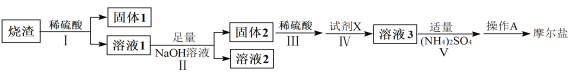
(1)写出试剂X的化学式__________。
(2)写出“溶液1”中某种离子与NaOH反应生成“溶液2”中离子的离子方程式________。
(3)操作A为蒸发浓缩至_________、冷却结晶、过滤、洗涤、干燥。其中过滤操作可用如图装置进行,请选择合适的编号,按正确的操作顺序补充完整(洗涤操作只需考虑一次):开抽气泵→a→b→d→_________→d→c→关抽气泵。
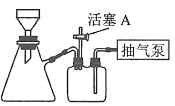
a.转移固液混合物
b.关活塞A
c.开活塞A
d.确认抽干
e.加洗涤剂洗涤
(4)实验制得的摩尔盐的纯度可用Ce(SO4)2标准溶液滴定进行测定。滴定反应为Fe2++Ce4+=Fe3++Ce3+。测定时,先称取4.000g样品,配成100mL溶液,取出其中20.00mL放入锥形瓶中,对溶液进行必要处理后,用0.1000mol·L-1Ce(SO4)2标准溶液滴定至终点,记录数据如下表:
滴定次数 | 0.1000mol·L-1Ce(SO4)2标准溶液体积(mL) | |
滴定前读数 | 滴定后读数 | |
1 | 0.10 | 20.12 |
2 | 0.12 | 20.10 |
3 | 0.05 | 21.65 |
①产品中摩尔盐的纯度为__________(用质量分数表示,保留4位有效数字)。
②若滴定过程中没有润洗滴定管,则会造成样品纯度______(填“偏高”、“偏低”或“无影响”)