题目内容
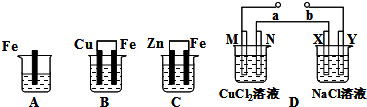
A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸.

(1)B中正极的电极反应式为
(2)C中被腐蚀的金属是
(3)A、B、C中铁被腐蚀的速率,由快到慢的顺序是

(1)B中正极的电极反应式为
2H++2e-=H2↑
2H++2e-=H2↑
.(2)C中被腐蚀的金属是
Zn
Zn
,负极的电极反应式为Zn-2e-=Zn2+
Zn-2e-=Zn2+
.(3)A、B、C中铁被腐蚀的速率,由快到慢的顺序是
B>A>C
B>A>C
.分析:(1)铁做负极,铜做正极,电解质溶液为硫酸,则正极反应为2H++2e-=H2↑;
(2)锌比铁活泼,做原电池的负极而被氧化,负极反应为Zn-2e-=Zn2+;
(3)电化学腐蚀的速率大于化学腐蚀的速率,金属做原电池正极时得到保护.
(2)锌比铁活泼,做原电池的负极而被氧化,负极反应为Zn-2e-=Zn2+;
(3)电化学腐蚀的速率大于化学腐蚀的速率,金属做原电池正极时得到保护.
解答:解:(1)B中铁做负极,铜做正极,电解质溶液为硫酸,则正极反应为2H++2e-=H2↑,故答案为:2H++2e-=H2↑;
(2)C形成原电池,锌比铁活泼,做原电池的负极而被氧化,负极反应为Zn-2e-=Zn2+,
故答案为:Zn,Zn-2e-=Zn2+;
(3)A发生化学腐蚀,B发生电化学腐蚀,C锌比铁活泼,铁做原电池的正极而被保护,电化学腐蚀的速率大于化学腐蚀的速率,故答案为:B>A>C.
(2)C形成原电池,锌比铁活泼,做原电池的负极而被氧化,负极反应为Zn-2e-=Zn2+,
故答案为:Zn,Zn-2e-=Zn2+;
(3)A发生化学腐蚀,B发生电化学腐蚀,C锌比铁活泼,铁做原电池的正极而被保护,电化学腐蚀的速率大于化学腐蚀的速率,故答案为:B>A>C.
点评:本题考查金属的电化学腐蚀与防护,题目难度不大,注意金属的电化学腐蚀与化学腐蚀的区别,以及比较金属腐蚀快慢的方法.

练习册系列答案
相关题目