题目内容
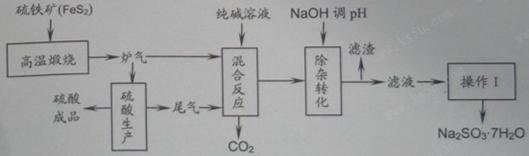
抗氧剂亚硫酸钠可利用硫酸工业的炉气和尾气与纯碱反应来制取,生产流程如下图:

己知:①炉气、尾气中均含有SO2、水蒸气等;②“混合反应”中还溶解有少量Fe2O3、MgO等矿尘。
(1)“混合反应”中纯碱(Na2CO3)参与反应的化学方程式为:
________________ (任写一个)。
(2)用NaOH“除杂”时,主要的离子方程式为:
________ (任写一个)。
(3)通过“操作I”可以得到亚硫酸钠晶体,其操作过程包括:加热蒸发浓缩、
(写出主要步骤名称)及洗涤、干燥。
 (4)硫酸生产中炉气转化反应为:2SO2(g)+O2(g)
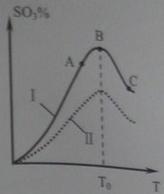
(4)硫酸生产中炉气转化反应为:2SO2(g)+O2(g)![]() 2SO3(g)。研究发现,SO3的体积分数(SO3%)随温度(T)的变化如曲线I所示。
2SO3(g)。研究发现,SO3的体积分数(SO3%)随温度(T)的变化如曲线I所示。
下列判断正确的是__________(填序号)。
A.该反应的正反应为放热反应
B.曲线I上A、C两点反应速率的关系是:υA>υC
C.反应达到B点时,2υ正(O2)=υ逆(SO3)
D.已知V2O5的催化效果比Fe2O3好,若I表示用V2O5催化剂的曲线,则II是Fe2O3作催化剂的曲线
(1)SO2+Na2CO3=Na2SO3+CO2↑(或2SO2+Na2CO3+H2O=2NaHSO3+CO2↑)
(2)Fe2++2OH-=Fe(OH)2↓(或Mg2++2OH-=Mg(OH)2↓;或HSO3-+OH-=SO32-+H2O))
(3)冷却结晶、过滤
(4)AC

练习册系列答案
相关题目


 2SO3(g)。研究发现,SO3的体积分数(SO3%)随温度(T)的变化如曲线Ⅰ所示。下列判断正确的是________
2SO3(g)。研究发现,SO3的体积分数(SO3%)随温度(T)的变化如曲线Ⅰ所示。下列判断正确的是________



 2SO3(g)。研究发现,SO3的体积分数(SO3%)随温度(T)的变化如曲线Ⅰ所示。下列判断正确的是________
2SO3(g)。研究发现,SO3的体积分数(SO3%)随温度(T)的变化如曲线Ⅰ所示。下列判断正确的是________

