题目内容
6.二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构中每个原子均满足8电子结构,常温下,S2Cl2就是一种橙黄色的液体,易与水反应,并产生能使品红褪色的气体.下列说法中错误的是( )| A. | S2Cl2中的硫元素显+1 价 | |
| B. | S2Cl2属于共价化合物 | |
| C. | S2Cl2与水的反应属于复分解反应 | |
| D. | S2Cl2与H2O反应的生成物中可能有S |
分析 S2Cl2中的硫元素显+1 价,氯元素化合价为-1价,为共价化合物,易与水反应,并产生能使品红褪色的气体,该气体为二氧化硫,说明S元素化合价发生变化,为歧化反应,S元素化合价由-1价变为+4价,0价,反应的方程式为2S2Cl2+2H2O=SO2↑+3S↓+4HCl,以此解答该题.
解答 解:A.氯元素在S2Cl2中为-1价,根据化合价规则知硫元素的化合价为+1价,故A正确;
B.S2Cl2为非金属元素形成的共价化合物,故B正确;
C.与水反应产生能使品红褪色的气体,该气体为二氧化硫,说明S元素化合价发生变化,为氧化还原反应,故C错误;
D.S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O=SO2↑+3S↓+4HCl,故D正确.
故选C.
点评 本题以S2Cl2的结构为载体,考查分子结构、化学键、氧化还原反应等,难度不大,是对基础知识的综合运用与学生能力的考查,注意基础知识的全面掌握,是一道不错的能力考查题目.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.下列是有关生活中的醋酸,其中主要利用了醋酸酸性的是( )
①醋酸不小心滴到大理石桌面上,桌面失去光泽
②熏醋可一定程度上防止流行性感冒
③醋可以除去水壶上的水垢
④用醋和酒烹饪鱼,除去鱼的腥味.
①醋酸不小心滴到大理石桌面上,桌面失去光泽
②熏醋可一定程度上防止流行性感冒
③醋可以除去水壶上的水垢
④用醋和酒烹饪鱼,除去鱼的腥味.
| A. | ①③④ | B. | ②④ | C. | ①④ | D. | ②③ |
9.下列说法正确的是( )
| A. | 干冰升华时要吸收热量,所以这是吸热反应 | |
| B. | 浓硫酸可用来干燥SO2、CO、Cl2等气体 | |
| C. | 浓硫酸具有强氧化性,常温下不可用铝罐盛装 | |
| D. | 二氧化硫能使滴有酚酞的氢氧化钠溶液褪色,体现了其漂白性 |
6.一定条件下,容积为1L的密闭容器中发生反应:2SO2(g)+O2(g)?2SO3(g),下列各项中不能说明该反应已达化学平衡状态的是( )
| A. | 消耗2 mol SO2的同时生成1 mol O2 | |
| B. | 容器内气体总物质的量不再变化 | |
| C. | 反应平衡常数保持不变 | |
| D. | SO3的气体体积分数不再变化 |
11.某小组为研究电化学原理,设计如图装置,下列叙述不正确的是( )
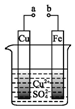

| A. | a和b用导线连接时,铜片上发生的反应为:Cu2++2e-═Cu | |
| B. | a和b不连接时,铁片上会有红色铜析出 | |
| C. | a和b分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动 | |
| D. | 无论a和b是否连接,铁片均会溶解,溶液均从蓝色逐渐变成浅绿色 |
18.下列叙述正确的是( )
| A. | 加热能够抑制水的电离 | |
| B. | 金属发生吸氧腐蚀时,被腐蚀的速率和氧气浓度无关 | |
| C. | 原电池中发生的反应达到平衡时,该电池仍有电流产生 | |
| D. | 在同浓度的盐酸中,ZnS可溶而CuS不溶,说明CuS的溶解度比ZnS的小 |
16.设NA为阿伏加德罗常数的数值.下列有关叙述不正确的是( )
| A. | 44 g乙醛中所含的氧原子数为NA | |
| B. | 常温常压下,8gCH4含有5 NA个电子 | |
| C. | 标准状况下,22.4L苯含有NA个C6H6分子 | |
| D. | 14 g乙烯中所含的C-H键数目为2NA |

 .
.