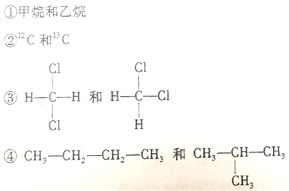
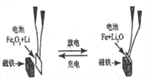
题目内容
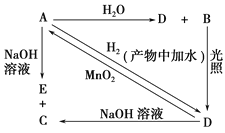
【题目】已知A、B、C、D、E、F是含有同一种元素的化合物,其中F是能使湿润的红色石蕊试纸变蓝的气体,它们之间能发生如下反应:①A+H2O→B+C;②C+F→D;③D+NaOH![]() F+E+H2O。
F+E+H2O。
(1)写出它们的化学式:A________、C________、D________、F________。
(2)写出下列反应的离子方程式,并按要求填空:
①_____________,这个反应的氧化剂是________,还原剂是________;
③____________________________。
(3)工业生产C的过程中有如下一步反应,即F经催化氧化生成B和H2O,写出该步反应的化学方程式________。
【答案】 NO2 HNO3 NH4NO3 NH3 3NO2+H2O=2H++2NO3—+NO NO2 NO2 NH4++OH![]() NH3↑+H2O 4NH3+5O2
NH3↑+H2O 4NH3+5O2![]() 4NO+6H2O
4NO+6H2O
【解析】
A、B、C、D、E、F是含有同一种元素的化合物,F是能使湿润的红色石蕊试纸变蓝的气体,则F是NH3,它们之间能发生如下反应:③D+NaOH![]() F+E+H2O,说明D是铵盐,E为钠盐,且A、B、C、D、E、F是含有同一种元素的化合物,则E是NaNO3,D是NH4NO3,根据②C+F→D知,C是HNO3,根据①A+H2O→B+C知,且A和B、C都含有同一种元素,则A是NO2,B是NO,根据物质的性质分析解答。
F+E+H2O,说明D是铵盐,E为钠盐,且A、B、C、D、E、F是含有同一种元素的化合物,则E是NaNO3,D是NH4NO3,根据②C+F→D知,C是HNO3,根据①A+H2O→B+C知,且A和B、C都含有同一种元素,则A是NO2,B是NO,根据物质的性质分析解答。
(1)由上分析,A为NO2,B为NO,C为HNO3,D为NH4NO3,E为NaNO3,F为NH3;
(2)①二氧化氮和水反应生成一氧化氮和硝酸,离子方程式为:3NO2+H2O=2H++2NO3—+NO,该反应中N元素化合价由+4价变为+2价和+5价,所以此反应中氧化剂、还原剂均是NO2;
③为硝酸铵与氢氧化钠反应,方程式为NH4++OH![]() NH3↑+H2O;
NH3↑+H2O;
(3)NH3经催化氧化生成NO和H2O,反应的化学方程式为4NH3+5O2![]() 4NO+6H2O。
4NO+6H2O。