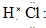题目内容
镁是一种非常重要的金属,其单质及化合物在航空航天、汽车制造、医药、添加剂、建筑等方面都有非常广泛的应用.(1)工业上常用电解熔融MgCl2制备金属镁,而MgCl2的获得主要有两种方法:
方法一:从海水或光卤石中先获得MgCl2?6H2O,然后制得无水MgCl2.
方法二:MgCO3
| ||
| ||
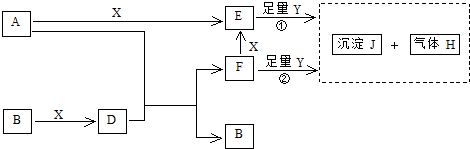
则:
在“方法一”中,从MgCl2?6H2O制无水MgCl2操作时应在
在“方法二”中,MgO和C能否直接反应生成金属镁?答:
(2)镁电池在性能上优于其他电池,具有更安全、环保、能效高等优点.有一种镁电池的反应为:Mg+2CuCl═2Cu+MgCl2,又知CuCl难溶于水,则该电池的正极反应式是
(3)化合物MgSO4在医疗上具有镇静、抗痉挛等功效.有一种以菱镁矿(主要成份是MgCO3)为主要原料制备MgSO4的方法如下:
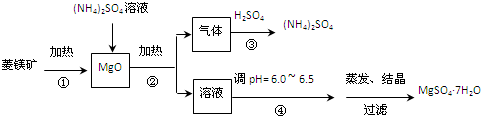
步骤②中发生反应的离子方程式为
步骤④中调节pH=6.0~6.5的目的是
对MgSO4?7H2O晶体直接加热是否能得到无水MgSO4固体?答:
镁很活泼,在加热条件下会与空气中的氧气和二氧化碳反应,不能用镁和碳直接反应得到镁;
(2)镁电池属于原电池,正极CuCl得电子生成Cu;
(3)步骤②中发生反应的为硫酸铵和氧化镁反应生成氨气、硫酸镁和水,步骤④中将硫酸镁溶液蒸发、结晶时,调节pH为弱酸性,抑制镁离子的水解;将MgSO4?7H2O晶体直接加热,硫酸镁较稳定,结晶水脱去,硫酸镁可以稳定存在.
镁很活泼,在加热条件下会与空气中的氧气和二氧化碳反应,回到氧化镁,所以不能用镁和碳直接反应得到镁,
故答案为:HCl气;否;
(2)镁电池属于原电池,正极得电子,是还原反应,Mg+2CuCl═2Cu+MgCl2 中得电子的是CuCl生成Cu,
故答案为:2CuCl+2e-═2Cu+2Cl-;
(3)步骤②中发生反应的为硫酸铵和氧化镁反应生成氨气、硫酸镁和水,改写成离子方程式为 2NH4++MgO═Mg2++2NH3↑+H2O;
步骤④中将硫酸镁溶液蒸发、结晶时,为了抑制镁离子的水解,调节pH为弱酸性,使镁离子的水解平衡逆向移动,得到纯净的硫酸镁晶体;
将MgSO4?7H2O晶体直接加热会造成结晶水脱去,硫酸镁较稳定,可以稳定存在.
故答案为:2NH4++MgO═Mg2++2NH3↑+H2O;抑制Mg2+水解,为了得到较纯的产品;能.

 教材全解字词句篇系列答案
教材全解字词句篇系列答案已知:乙醇是一种非常重要的烃的衍生物,是无色有特殊气味的液体。丰中化学兴趣小组对乙醇的结构和性质进行了以下探究,请你参与并完成对有关问题的解答。
![]() 【观察与思考】(1)乙醇分子的核磁共振氢谱有 个吸收峰。
【观察与思考】(1)乙醇分子的核磁共振氢谱有 个吸收峰。
![]() 【活动与探究】
【活动与探究】
![]() (2)甲同学向小烧杯中加入无水乙醇,再放入一小块金属钠(约绿豆粒大),观察实验现
(2)甲同学向小烧杯中加入无水乙醇,再放入一小块金属钠(约绿豆粒大),观察实验现
![]() 象。请在下表中将观察到的实验现象及结论补充完全(有多少现象等就填多少,不必填满)。
象。请在下表中将观察到的实验现象及结论补充完全(有多少现象等就填多少,不必填满)。
| 实验现象 | 结 论 |
① | 钠沉在乙醇下面 | 钠的密度大于乙醇 |
② |
|
|
|
|
|
|
|
|
 (3)乙同学向试管中加入3~4 mL无水乙醇,浸入50℃左右的热水中,再将铜丝烧至红热,迅速插入乙醇中,欲验证此实验的有机产物,可以将产物加入盛有 的试管中并在酒精灯火焰上直接加热煮沸,观察现象即可,此反应的化学方程式为 。
(3)乙同学向试管中加入3~4 mL无水乙醇,浸入50℃左右的热水中,再将铜丝烧至红热,迅速插入乙醇中,欲验证此实验的有机产物,可以将产物加入盛有 的试管中并在酒精灯火焰上直接加热煮沸,观察现象即可,此反应的化学方程式为 。
【交流与讨论】
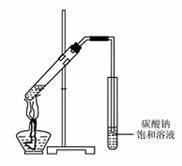
(4)丙同学向一支试管中加入3 mL 乙醇,然后边摇动试管边慢慢加入2 mL浓硫酸和2 mL冰醋酸,按右图所示连接好装置,请指出该装置的主要错误是 。
已知:乙醇是一种非常重要的烃的衍生物,是无色有特殊气味的液体。丰中化学兴趣小组对乙醇的结构和性质进行了以下探究,请你参与并完成对有关问题的解答。
![]() 【观察与思考】(1)乙醇分子的核磁共振氢谱有 个吸收峰。
【观察与思考】(1)乙醇分子的核磁共振氢谱有 个吸收峰。
![]() 【活动与探究】
【活动与探究】
![]() (2)甲同学向小烧杯中加入无水乙醇,再放入一小块金属钠(约绿豆粒大),观察实验现
(2)甲同学向小烧杯中加入无水乙醇,再放入一小块金属钠(约绿豆粒大),观察实验现
![]() 象。请在下表中将观察到的实验现象及结论补充完全(有多少现象等就填多少,不必填满)。
象。请在下表中将观察到的实验现象及结论补充完全(有多少现象等就填多少,不必填满)。
| 实验现象 | 结 论 |
① | 钠沉在乙醇下面 | 钠的密度大于乙醇 |
② |
|
|
|
|
|
|
|
|
 (3)乙同学向试管中加入3~4 mL无水乙醇,浸入50℃左右的热水中,再将铜丝烧至红热,迅速插入乙醇中,欲验证此实验的有机产物,可以将产物加入盛有 的试管中并在酒精灯火焰上直接加热煮沸,观察现象即可,此反应的化学方程式为 。
(3)乙同学向试管中加入3~4 mL无水乙醇,浸入50℃左右的热水中,再将铜丝烧至红热,迅速插入乙醇中,欲验证此实验的有机产物,可以将产物加入盛有 的试管中并在酒精灯火焰上直接加热煮沸,观察现象即可,此反应的化学方程式为 。
【交流与讨论】
(4)丙同学向一支试管中加入3 mL 乙醇,然后边摇动试管边慢慢加入2 mL浓硫酸和2 mL冰醋酸,按右图所示连接好装置,请指出该装置的主要错误是 。