题目内容
将镁条在二氧化碳气体中充分燃烧后的产物全部加入50 mL 1.8 mol.L-1的盐酸中,充分振荡后,过滤,向滤液中加入过量的氢氧化钠溶液,生成0.58 g沉淀。求镁条的质量。
答案:
解析:
解析:
| Mg条质量0.24 g。利用关系式和题意知0.58
g沉淀即为Mg(OH)2。Mg~MgO~2HCl
2HCl ~ Mg ~ MgCl2 ~ Mg(OH)2 2 mol 1 mol 58 g Cl-来自于HCl 0.02 mol 0.01mol 0.58 g 恰好生成这些沉淀时需的Mg2+对应的,所以0.02 mol Cl-<0.05×1.8=0.09 mol Cl-,原Mg条全部反应,0.09 mol HCl过量,∴Mg条质量为0.24 g,在此题中要注意多步反应中元素守恒和反应物选量的计算。
|

练习册系列答案
相关题目
下列叙述不正确的是( )
| A、镁条能在二氧化碳气体中燃烧 | B、工业上可用氯气和石灰乳为原料制造漂白粉 | C、电解氯化钠溶液可以制得钠单质和氯气 | D、将盛有氢氧化铁胶体的烧杯置于暗处,用一束光照射,从垂直于光线的方向可以观察到一条光亮的通路 |
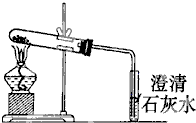 镁将成为21世纪重要的轻型环保材料.
镁将成为21世纪重要的轻型环保材料.