题目内容
X、Y、Z、W为含有相同电子数的分子或离子,均由原子序数小于10的元素组成,X有5个原子核.通常状况下,W为无色液体.
已知:X+Y![]() Z+W
Z+W
(1)Y的电子式是________.
(2)液态Z和W的电离相似,都可电离出电子数相同的两种离子,液态Z的电离方程式是________.
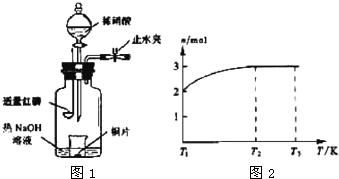
(3)用图示装置制备NO并验证其还原性.有下列主要操作:
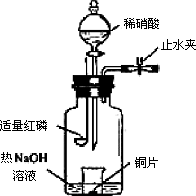
a.向广口瓶内注入足量热NaOH溶液,将盛有铜片的小烧杯放入瓶中.
b.关闭止水夹,点燃红磷,伸入瓶中,塞好胶塞.
c.待红磷充分燃烧,一段时间后打开分液漏斗旋塞,向烧杯中滴入少量稀硝酸.
①步骤c后还缺少的一步主要操作是________.
②红磷充分燃烧的产物与NaOH溶液反应的离子方程式是________.
③步骤c滴入稀硝酸后烧杯中的现象是________.反应的离子方程式是________.
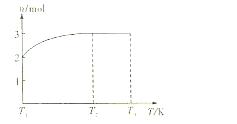
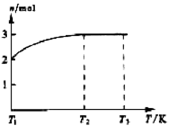
(4)一定温度下,将1 mol N2O4置于密闭容器中,保持压强不变,升高温度至T1的过程中,气体由无色逐渐变为红棕色.温度由T1继续升高到T2的过程中,气体逐渐变为无色.若保持T2,增大压强,气体逐渐变为红棕色.气体的物质的量n随温度T变化的关系如图所示.
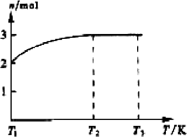
①温度在T1T2之间,反应的化学方程式是________.
②温度在T2T3之间,气体的平均相对分子质量是(保留1位小数)________.
答案:
解析:
解析:
|
(1) (2)2NH3(l) (3)①打开止水夹,通入少量氧气(2分) ②P2O5+6OH-=2PO43-+3H2O(2分) ③Cu片逐渐溶解,有无色气泡产生,溶液由无色变为蓝色(3分) 3Cu+8H++2NO (4)①2NO ②30.7(2分) |

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 X、Y、Z、W为含有相同电子数的分子或离子,均由原子序数小于10的元素组成.X有5个原子核.通常状况下,W为无色液体.已知:X+Y
X、Y、Z、W为含有相同电子数的分子或离子,均由原子序数小于10的元素组成.X有5个原子核.通常状况下,W为无色液体.已知:X+Y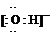
 (2008?北京)X、Y、Z、W为含有相同电子数的分子或离子,均由原子序数小于10的元素组成,X有5个原子核.通常状况下,W为无色液体.
(2008?北京)X、Y、Z、W为含有相同电子数的分子或离子,均由原子序数小于10的元素组成,X有5个原子核.通常状况下,W为无色液体.
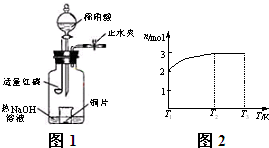
 (3)用图示装置制备NO并验证其还原性。有下列主要操作:
(3)用图示装置制备NO并验证其还原性。有下列主要操作: (4)一定温度下,将1 mol N2O4置于密闭容器中,保持压强不变,升高温度至T1的过程中,气体由无色逐渐变为红棕色。温度由T1继续升高到T2的过程中,气体逐渐变为无色。若保持T2,增大压强,气体逐渐变为红棕色。气体的物质的量n随温度T变化的关系如图所示。
(4)一定温度下,将1 mol N2O4置于密闭容器中,保持压强不变,升高温度至T1的过程中,气体由无色逐渐变为红棕色。温度由T1继续升高到T2的过程中,气体逐渐变为无色。若保持T2,增大压强,气体逐渐变为红棕色。气体的物质的量n随温度T变化的关系如图所示。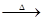 Z+W
Z+W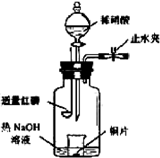
 Z+W
Z+W