��Ŀ����
��09�γǵ����ε��У���ȸʯ����Ҫ�ɷ���Cu(OH)2?CuCO3 ����������ҪΪFeCO3�ȣ������������ڵ�����ʵ�鲽�����£�
����100 mL�ձ��м���3 mol?L��1ϡ����12 mL�����ȣ�������μ���5~10 g��ȸʯ�ۣ���������ͭ��Һ��pHԼΪ1.5��2.0������ˮϡ����35 mL���ҡ�
�ڵμ�Լ4 mL 3% H2O2�����μ������2 mol? L��1 NaOH��Һ������Һ����ȣ�����pHֵΪ3.0��3.5������Һ�������������ӣ����ȹ��ˡ�
��ˮԡ���ȣ������ᾧ
���ؽᾧ
�Իش��������⣺
��1���������ΪʲôҪ������μ����ȸʯ��? ���������ȡ�Ļ�ѧ����ʽ�� ��
��2��pHֵ����Ϊ3.0��3.5����Ŀ���ǣ� ���ӹ������ⷢ����Ӧ�����ӷ���ʽΪ�� ��
��3��Ϊʲô����ˮԡ���ȼ������ж�����Ũ������ɣ� ��
��4�����Ƶõ���Ʒ�������ǽ������ط�����������ԭ�������ؼ�¼���±���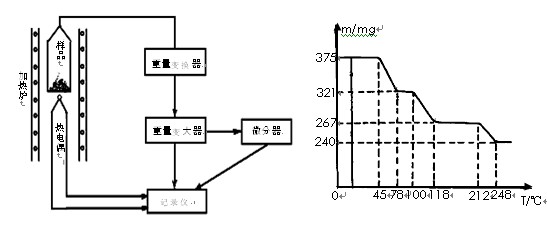
д��212��250���¶ȷ�Χ�ڷ�����Ӧ�Ļ�ѧ����ʽ: ��
��1��ԭ����Cu(OH)2?CuCO3�ĺ���δ֪��������μӿ���ʹ���߽ӽ�����ȫ��Ӧ����������һ�ֹ���̫�ࣻ���Կ��ƺ��ʵ�pHֵ�����ٺ��������������Ƶļ��������Ӷ��������ʵ����롣
Cu(OH)2?CuCO3 + 2H2SO4 = 2CuSO4 + 3H2O + CO2��
��2��ʹFe3+������ȫ����Cu2+������ĸҺ�У�2Fe2+ +2H2O2+2H+=2Fe3++2H2O
��3�� ���¶ȸ�ʱ��CuSO4?5H2O��ʧȥ�ᾧˮ����Һ����ֽ϶ྦྷĤʱ����˵������Ũ������ɡ�
��4��CuSO4?H2O
��09�γǵ����ε��У��Ȼ����dz�����ˮ����������ˮFeCl3���۵�Ϊ555K���е�Ϊ588K����ҵ���Ʊ���ˮFeCl3��һ�ֹ������£�
��1��ȡ0.5mL���Ȼ�����Һ����50mL��ˮ�У������Ƭ�̵ú��ɫ��Һ�壬�ù��̿������ӷ���ʽ��ʾΪ�� ��
��2����֪��ˮ���Ȼ�����ˮ�е��ܽ�����£�
�¶�/��. | 0 | 10 | 20 | 30 | 50 | 80 | 100 |
�ܽ��(g/100gH20) | 74.4 | 81.9 | 91.8 | 106.8 | 315.1 | 525.8 | 535.7 |
��FeCl3��Һ�л��FeCl3?6H2O�ķ����ǣ� ��
��3�����������¶ȳ���673K��������Է�������Ϊ325�����ʣ������ʵķ���ʽΪ�� ��
��4������ʱ��FeCl3��Һ�еμ�NaOH��Һ������ҺpHΪ2.7ʱ��Fe3+��ʼ����������ҺpHΪ4ʱ��c(Fe3+)= mol/L����֪��Ksp[Fe(OH)3]= 1.1��10��36����
��5�����ռ�X��: �������������ռ�X�������ǣ� ��
��6��FeCl3����������ͨ�����õ������ⶨ����ȡmg��ˮ�Ȼ�����Ʒ������ϡ���ᣬ��ת�Ƶ�100mL����ƿ��������ˮ���ݣ�ȡ��10.00mL�������Թ�����KI��Һ����ַ�Ӧ���õ�����ָʾ������cmol/LNa2S2O3��Һ�ζ���I2+2S2O32��=2I�� +S4O62����������ȥVmL������Ʒ���Ȼ�������������Ϊ�� ��
��09�γǵ����ε��У�����X��Y��Z�����л���(����Է���������С��100)�����Ǻ�̼���⡢������4��Ԫ���е����ֻ����֡���һ����ѧϰС���ͬѧ��ȷ�����ǵ���ɻ�ṹ��
��1���ⶨ�л�����Է����������õķ���ͨ���� ������ţ���ͬ���ٺ�����ף������ף�����˴Ź����ף���
Ԫ�ط��������������ʵ���˴Ź�����ֻ��һ�����շ���ǣ�
![]()
![]()
![]()
![]()
![]()
![]() ���� �����飬 �� �� �� �� �� ��
���� �����飬 �� �� �� �� �� ��
![]()
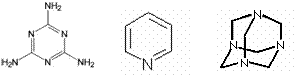
![]() ��2��X��C��H��O��N����Ԫ����ɣ���(N)=18.67%����X���������ᷴӦ����������������Һ��Ӧ����X���ܵĽṹ��ʽΪ�� ��
��2��X��C��H��O��N����Ԫ����ɣ���(N)=18.67%����X���������ᷴӦ����������������Һ��Ӧ����X���ܵĽṹ��ʽΪ�� ��
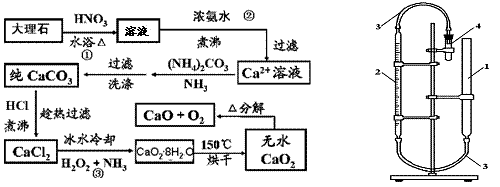
��3��Y��Z����Է���������ȣ�������ȫȼ��ʱ��ֻ������CO2��H2O��N2�е����ֻ����֡�ijͬѧȡһ������Y��Z�Ļ�����ȫȼ��ʱ�ڱ�״���µ�ʵ�������£�
ʵ����� | ����� ���� | ���ʵ�����ϵn(Y)/n(Z) | ������� | ||
m(CO2)/g | m(H2O)/g | V(N2)/mL | |||
�� | 3g | 2��3 | 3.08 | 1.8 | 672 |
�� | 3g | 3��2 | 3.52 | 1.8 | 448 |

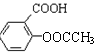 ��
��