题目内容
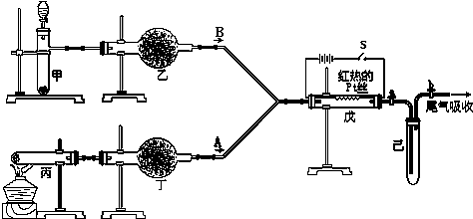
课外小组设计了如图所示的实验装置,进行气体性质实验.图中箭头表示气体流向.A表示一种纯净、干燥的气体,B是另一种气体,反应进行一段时间后,装置己中有红棕色气体生成.实验中所用的药品和干燥剂只能从下列物质中选取:Na2CO3、NaHCO3、MnO2、Na2O2、NaCl、无水CaCl2、NH4HCO3、碱石灰等固体,H2O2、蒸馏水.

根据图中装置和反应现象回答:
(1)充分反应后丙中无固体物质剩余,发生反应的化学方程式为
________________________________________________________________________.
(2)丁中的干燥剂应选__________,不选另一种干燥剂的理由是
________________________________________________________________________.
(3)甲中发生反应的化学方程式为________________________________________.
(4)观察到反应开始后断开电键K,铂丝能继续保持红热、戊中发生的主要反应的化学
方程式为______________________,此反应是__________(吸热、放热)反应.
(5)若装置的气密性良好,甲、丙中均有气体产生,其余操作正常,但己中未观察到红
棕色,可能的原因是___________________________________________________
________________________________________________________________________.
解析:根据所给药品及装置特点分析:A是NH3,B是O2.在戊中发生的反应是4NH3
+5O2![]() 4NO+6H2O,若要在己中看到红棕色气体,必须让O2过量,发生反应
4NO+6H2O,若要在己中看到红棕色气体,必须让O2过量,发生反应
为2NO+O2===2NO2.
答案:(1)NH4HCO3![]() NH3↑+CO2↑+H2O↑
NH3↑+CO2↑+H2O↑
(2)碱石灰 无水CaCl2只能吸水,不能吸收CO2(或CaCl2能吸收NH3)
(3)2H2O2![]() 2H2O+O2↑(或2Na2O2+2H2O===4NaOH+O2↑)
2H2O+O2↑(或2Na2O2+2H2O===4NaOH+O2↑)
(4)4NH3+5O2![]() 4NO+6H2O 放热
4NO+6H2O 放热
(5)甲装置产生的氧气量不足

 阅读快车系列答案
阅读快车系列答案
| 瓶Ⅰ | 瓶Ⅱ |
A | Ca(OH)2 | KOH |
B | NaOH | Ca(OH)2 |
C | 稀盐酸 | AgNO3 |
D | NaOH | KOH |

 4NO+6H2O
4NO+6H2O
