题目内容
13.下列化合物的分子中,所有原子都处于同一平面的是( )| A. | 四氟乙烯 | B. | 甲苯 | C. | 乙酸 | D. | 甲烷 |
分析 在常见的有机化合物中甲烷是正四面体结构,乙烯和苯是平面型结构,乙炔是直线型结构,其它有机物可在此基础上进行判断.
解答 解:A、乙烯具有平面型结构,四氟乙烯可看作是一个氟原子取代乙烯中的四个氢原子,所有原子在同一个平面,故A正确;
B、甲苯中的甲基中的H原子和苯环不能全部处于同一平面上,故B错误;
C、乙酸中甲基上的H原子不能全部和-COOH中的原子共平面,故C错误;
D、甲烷中的原子呈现四面体构型,能全部在同一平面上,故D错误.
故选A.
点评 本题主要考查有机化合物的结构特点,做题时注意从甲烷、乙烯、苯和乙炔的结构特点判断有机分子的空间结构.

练习册系列答案
 目标测试系列答案
目标测试系列答案
相关题目
4.现有部分短周期元素的原子结构如表:
(1)写出X的元素符号:N,元素Y的最简单氢化物的化学式为CH4.
(2)Z元素原子的质量数为23.
(3)X和Z两种元素的最高价氧化物对应的水化物相互反应的离子方程式为H++OH-=H2O.
(4)Y和Z两种元素的最高价氧化物发生氧化还原反应的化学方程式2CO2+2Na2O2=2Na2CO3+O2
(5)W、X、Y、Z为短周期内除稀有气体元素外的四种元素.它们的原子序数依次增大,其中只有Y是金属元素,Y的最外层电子数和W最外层电子数相等,Y、Z两元素的质子数之和为W、X两元素的质子数之和的3倍.由此可知元素W为H;X为O;Y 为Na;Z为S.上述元素中任意三种可组成盐,写出这些盐的化学式Na2SO4、Na2SO3、Na2S2O3、NaHS.
| 元素符 号 | 元素原子结构 |
X | 原子结构示意图为  |
| Y | 最外层电子数是次外层电子数的2倍 |
Z | 原子核内含有12个中子,且其离子的结构示意图为  |
(2)Z元素原子的质量数为23.
(3)X和Z两种元素的最高价氧化物对应的水化物相互反应的离子方程式为H++OH-=H2O.
(4)Y和Z两种元素的最高价氧化物发生氧化还原反应的化学方程式2CO2+2Na2O2=2Na2CO3+O2
(5)W、X、Y、Z为短周期内除稀有气体元素外的四种元素.它们的原子序数依次增大,其中只有Y是金属元素,Y的最外层电子数和W最外层电子数相等,Y、Z两元素的质子数之和为W、X两元素的质子数之和的3倍.由此可知元素W为H;X为O;Y 为Na;Z为S.上述元素中任意三种可组成盐,写出这些盐的化学式Na2SO4、Na2SO3、Na2S2O3、NaHS.
8.下列化合物中含3个“手性碳原子”的是( )
| A. |  | B. |  | C. |  | D. |  |
18.分子式为C5H10O2并能与饱和NaHCO3溶液反应放出气体的有机物有(不含量立体异构)( )
| A. | 8种 | B. | 6种 | C. | 5种 | D. | 4种 |
2.下列属于同位素的是( )
| A. | 红磷和白磷 | B. | ${\;}_{1}^{1}$H和${\;}_{1}^{2}$H | ||
| C. | H2O和D2O | D. | ${\;}_{8}^{16}$O和${\;}_{8}^{18}$O |
3.光纤广泛应用于现代通讯,制造光导纤维的基本原料是( )
| A. | CuO | B. | Al2O3 | C. | CaO | D. | SiO2 |

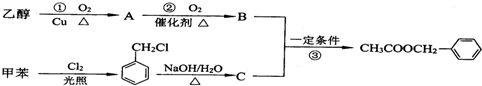
 +CH3COOH$→_{△}^{浓硫酸}$
+CH3COOH$→_{△}^{浓硫酸}$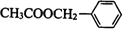 +H2O.
+H2O.