题目内容
【题目】选择下列物质填空
(1)①蔗糖溶液 ②盐酸 ③NH3 ④熔融BaSO4 ⑤Fe(OH)3胶体 ⑥液态HCl ⑦NH3·H2O ⑧金刚石 ⑨Cu。能导电的物质是______________,电解质是______________,非电解质是____________。
(2)已知3.01×1024个氖原子的质量为w g,则氖气的摩尔质量是_________。
(3)将V1L 0.1mol/L NaOH溶液与V2L 0.3mol/L Ba(OH)2溶液混合,所得溶液OH-浓度为0.3mol/L,如果混合后体积为混合前的体积和,则V1︰V2= ____________。
(4)气体化合物A分子式可表示为OxFy,已知同温同压下10 mL A受热分解生成15 mL O2和10 mL F2,则A的化学式为________。
【答案】 ②④⑤⑨ ④⑥⑦ ③ ![]() g·mol-1 3︰2 O3F2
g·mol-1 3︰2 O3F2
【解析】(1)含有自由移动电子或离子的物质可以导电,能导电的物质是盐酸、熔融BaSO4、Fe(OH)3胶体、Cu;溶于水或在熔融状态下能够自身电离出离子的化合物是电解质,属于电解质的是熔融BaSO4、液态HCl、NH3·H2O;于水和在熔融状态下都不能够自身电离出离子的化合物是非电解质,属于非电解质是氨气;(2)已知3.01×1024个氖原子的质量为w g,物质的量是3.01×1024÷6.02×1023/mol=5.0mol,则氖气的摩尔质量是![]() 。(3)根据混合过程中氢氧根的物质的量不变可知
。(3)根据混合过程中氢氧根的物质的量不变可知![]() ,解得V1︰V2=3︰2;(4)同温同压下10mLA受热分解生成15mLO2和10mLF2,则根据阿伏加德罗定律可知2OxFy=3O2+2F2,因此根据原子守恒可知A的化学式为O3F2。
,解得V1︰V2=3︰2;(4)同温同压下10mLA受热分解生成15mLO2和10mLF2,则根据阿伏加德罗定律可知2OxFy=3O2+2F2,因此根据原子守恒可知A的化学式为O3F2。

【题目】用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
实验序号 | A溶液 | B溶液 |
① | 20 mL 0.1 mol·L-1H2C2O4溶液 | 30 mL 0.01 mol·L-1KMnO4溶液 |
② | 20 mL 0.2 mol·L-1H2C2O4溶液 | 30 mL 0.01 mol·L-1KMnO4溶液 |

(1)该反应的离子方程式 。(已知H2C2O4是二元弱酸)
(2)该实验探究的是 因素对化学反应速率的影响。相同时间内针筒中所得CO2的体积大小关系是 < (填实验序号)。
(3)若实验①在2 min末收集了2.24 mL CO2(标准状况下),则在2 min末, c(MnO4-)=__________mol/L(假设混合液体积为50 mL)
(4)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定 来比较化学反应速率。(一条即可)
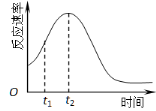 (5)小组同学发现反应速率总是如图,其中t1~t2时间内速率变快的主要原因可能是:
(5)小组同学发现反应速率总是如图,其中t1~t2时间内速率变快的主要原因可能是:

① ;② 。




