题目内容
如图所示装置,烧杯中盛有200mL 1mol?L-1的CuSO4溶液.负极为______,电极反应式为______.正极为______,电极反应式为______.

该原电池中,锌失电子变成离子进入溶液,发生氧化反应,电极反应式为:Zn-2e-=Zn2+,电子从锌片沿导线流向铜片,所以锌作负极,铜作正极,正极上铜离子得电子生成铜单质,发生还原反应,电极反应式为:Cu2++2e-=Cu.
故答案为:锌;Zn-2e-=Zn2+;铜;Cu2++2e-=Cu.
故答案为:锌;Zn-2e-=Zn2+;铜;Cu2++2e-=Cu.

练习册系列答案
相关题目
 如图所示装置
如图所示装置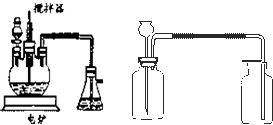 在中学化学实验中,通常用无水硫酸铜检验少量水的存在.由于无水硫酸铜吸湿性很强,需要现制现用.
在中学化学实验中,通常用无水硫酸铜检验少量水的存在.由于无水硫酸铜吸湿性很强,需要现制现用.

 下列有关实验原理或实验操作正确的是( )
下列有关实验原理或实验操作正确的是( )