题目内容
20.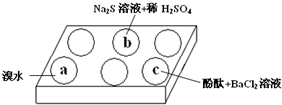 在白色点滴板上进行Na2SO3 的性质实验探究.如图所示,a、b、c三个凹槽中滴有Na2SO3 溶液,再分别滴加下图所示的试剂:
在白色点滴板上进行Na2SO3 的性质实验探究.如图所示,a、b、c三个凹槽中滴有Na2SO3 溶液,再分别滴加下图所示的试剂:(1)a中实验现象是溴水褪色,该现象可证明Na2SO3具有还原性.
(2)b中发生反应的离子方程式是SO32-+2S2-+6H+=3S↓+3 H2O.
(3)应用化学平衡原理解释c中现象(用化学用语及简单文字表述)在Na2SO3溶液中,SO32-水解显碱性:SO32-+H2O?HSO3-+OH-,所以滴入酚酞后溶液变红;在该溶液中加入BaCl2后,Ba2++SO32-═BaSO3↓(白色),由于c(SO32-)减小,SO32-水解平衡左移,c(OH-)减小,红色褪去.
(4)在用NaOH 溶液吸收SO2 的过程中,往往得到Na2SO3和NaHSO3 的混合溶液,溶液pH 随n(SO32-):n(HSO3-) 变化关系如表:
| n(SO3 2-):n(HSO3-) | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
a.c(Na+)+c(H+)=2c(SO32-)+c(HSO3-)+c(OH-)
b.c(Na+)>c(HSO3-)>c(SO32-)>c(OH-)>c(H+)
c.c(Na+)>c(SO32-)>c(HSO3-)>c(OH-)>c(H+)
②若n(SO32-):n(HSO3-)=3:2,则0.8mol NaOH溶液吸收了标准状况下的SO211.2 L.
分析 (1)Na2SO3 溶液中亚硫酸钠具有还原性和溴单质反应生成硫酸钠;
(2)Na2SO3 溶液与硫化钠、硫酸溶液发生氧化还原反应生成淡黄色硫单质沉淀;
(3)Na2SO3 溶液水解显碱性,使酚酞变红,加入氯化钡会结合亚硫酸根离子形成亚硫酸钡沉淀,水解平衡逆向进行,氢氧根离子浓度减小红色褪去;
(4)①当吸收液中n(SO32-):n(HSO3-)=10:1 时,依据图表分析,溶液呈碱性;
A、依据溶液中电荷守恒分析;
B、溶液中亚硫酸钠多溶液呈碱性,亚硫酸根离子大于亚硫酸氢根离子,钠离子浓度最大;
C、溶液中亚硫酸钠多溶液呈碱性,亚硫酸根离子大于亚硫酸氢根离子,钠离子浓度最大;
②若n(SO32-):n(HSO3-)=3:2,直平写出反应的离子方程式计算.
解答 解:(1)滴入溴水后褪色,说明亚硫酸钠具有还原性,被溴单质氧化为硫酸钠;
故答案为:溴水褪色;还原性;
(2)b中是滴入硫化钠溶液和稀硫酸,硫离子和亚硫酸根离子发生氧化还原反应生成淡黄色沉淀单质硫,发生反应的离子方程式是:SO32-+2S2-+6H+=3S↓+3 H2O;
故答案为:SO32-+2S2-+6H+=3S↓+3 H2O;
(3)d中滴入酚酞溶液变红,再加入BaCl2溶液后产生沉淀且红色褪去,在Na2SO3溶液中,SO32-水解显碱性:SO32-+H2O?HSO3-+OH-,所以滴入酚酞后溶液变红;在该溶液中加入BaCl2后,Ba2++SO32-═BaSO3↓(白色),水解平衡左移,氢氧根离子浓度减小,红色褪去;
故答案为:在Na2SO3溶液中,SO32-水解显碱性:SO32-+H2O?HSO3-+OH-,所以滴入酚酞后溶液变红;在该溶液中加入BaCl2后,Ba2++SO32-═BaSO3↓(白色),由于c(SO32-)减小,SO32-水解平衡左移,c(OH-)减小,红色褪去;
(4)①吸收液中n(SO32-):n(HSO3-)=10:1 时,依据图表数据分析判断,溶液呈碱性,亚硫酸钠物质的量大于亚硫酸氢钠
a、依据溶液中电荷守恒,c(Na+)+c(H+)=2c(SO32-)+c(HSO3-)+c(OH-);故a正确;
b、溶液中亚硫酸钠多溶液呈碱性,亚硫酸根离子大于亚硫酸氢根离子,钠离子浓度最大,离子浓度大小为:c(Na+)>c(SO32-)>c(HSO3-)>c(OH-)>c(H+)
;故b错误;
c、溶液中亚硫酸钠多溶液呈碱性,亚硫酸根离子大于亚硫酸氢根离子,钠离子浓度最大,离子浓度大小为:c(Na+)>c(SO32-)>c(HSO3-)>c(OH-)>c(H+)
;故c正确;
故答案为:ac;
②若n(SO32-):n(HSO3-)=3:2,反应物全部反应,直平得到反应方程式为:5SO2+8NaOH=2NaHSO3+3Na2SO3+3H2O,则0.8mol NaOH溶液吸收了标准状况下的SO2物质的量为0.5mol,标准状况体积为0.5mol×22.4L/mol=11.2L;
故答案为:11.2.
点评 本题考查了物质性质实验验证方法的分析判断,溶液中离子浓度大小比较,溶液中电荷守恒应用,化学方程式的计算分析,盐类水解平衡的影响因素判断,题目难度中等.

| A. | 甲醇、乙二醇 | B. | 甲酸乙酯和乙酸甲酯 | ||
| C. | 蚁酸和乙酸 | D. | 苯酚( -OH)和甲苯( -OH)和甲苯( -CH3) -CH3) |
| A. | Fe2O3 | B. | Fe(OH)3 | C. | FeO | D. | Fe3O4 |
(1)SO2是形成酸雨的元凶,它主要来源于煤和石油的燃烧.某实验小组采集酸雨
样品,随着时间的推移,多次测定该样品pH,得到了如下数据:
| 时间(h) | 开始 | 8 | 16 | 24 | 32 | 40 | 48 |
| pH | 5.0 | 4.8 | 4.5 | 4.3 | 4.2 | 4.0 | 4.0 |
②酸雨可导致下列哪些危害abd(填字母代号).
a.腐蚀建筑物 b.破坏农作物 c.造成洪涝灾害 d.使土壤、湖泊酸化
(2)在无机非金属材料中,硅及其化合物扮演着重要角色.
①实验室用于盛放碱性试剂的试剂瓶不用磨口玻璃塞.其原因是(用离子方程式表示)SiO2+2OH-═SiO32-+H2O;
②教材中有如下实验:取两个相同的滤纸条,分别放入蒸馏水和Na2SiO3饱和溶液中,使之充分吸湿、浸透,取出稍沥干(不再滴液)后,同时分别放置在酒精灯外焰处.观察到的现象如下表:
| 编号 | 实验 | 现象 |
| a | 放入蒸馏水 | 木条燃烧 |
| b | 放入Na2SiO3饱和溶液 | 木条不燃烧 |
(3)NO是大气污染物之一,近年来发现它有扩张血管,增强记忆的功能,因此成为生命科学的研究热点.
①汽车点火启动时产生的尾气是NO污染的主要来源,该反应的化学方程为N2+O2$\frac{\underline{\;放电\;}}{\;}$2NO;
②把NO气体压缩到1.01×107Pa,并加热到一定温度,发现气体压强迅速下降.当压强降至原来的$\frac{2}{3}$时,压强不再改变.已知,其中一种气体产物为N2O,则上述变化的化学方程式为3NO=N2O+NO2.
| A. | 实验①证明KClO3具有还原性 | |
| B. | 实验②中氧化剂与还原剂的物质的量之比为2:1 | |
| C. | 实验③说明KI被氧化 | |
| D. | 上述实验证明氧化性:ClO3->Cl2>I2 |
所用稀盐酸浓度为1.00mol•L-1、2.00mol•L-1,锌有细颗粒与粗颗粒两种规格,用量为6.50g.实验温度为298K、308K,每次实验稀盐酸的用量为25.0mL.
(1)完成以下实验设计(填写表格中空白项),并在实验目的一栏中填出对应的实验编号:
| 编号 | T/K | 锌规格 | 盐酸浓度/mol•L-1 | 实验目的 |
| ① | 298 | 粗颗粒 | 2.00 | (Ⅰ)实验①和②探究盐酸浓度对该反应速率的影响;(Ⅱ)实验①和 ③探究温度对该反应速率的影响;(Ⅲ)实验①和 ④探究锌规格(粗、细)对该反应速率的影响. |
| ② | 298 | |||
| ③ | 308 | |||
| ④ | 298 |
| 时间(S) | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| 氢气体积(mL) | 16.8 | 39.2 | 67.2 | 224 | 420 | 492.8 | 520.8 | 543.2 | 554.4 | 560 |
②反应速率最大的时间段(即0~10S、10~20S、20~30S、30~40S、40~50S、…)为40~50s,可能原因是反应放热;
③反应速率最小的时间段为90~100s,可能原因是盐酸浓度降低.
(3)另一学生也做同样的实验,由于反应太快,测量氢气的体积时不好控制,他就事先在硫酸溶液中分别加入等体积的下落溶液以减慢反应速率:
A.蒸馏水B.CuCl2溶液C.NaCl溶液
你认为他上述做法中可行的是AC(填相应字母).
| A. | H+、Ba2+、ClO-、SO42- | B. | Fe3+、H+、SO42-、I- | ||
| C. | Cu2+、NO3-、HCO3-、OH- | D. | K+、Ba2+、NO3-、Cl- |
| A. | 金属钠着火时,立即用沾水的毛巾覆盖 | |
| B. | 配制稀硫酸时将水倒入浓硫酸中并不断搅拌 | |
| C. | 不慎洒出的酒精在桌上着火时,立即用水扑灭 | |
| D. | 大量氯气泄漏时,迅速离开现场并尽量往高处去 |

 .
.