��Ŀ����
��1����2L���ܱ������з���4molN2O5���������·�Ӧ��2N2O5��g��
4NO2��g��+O2��g������Ӧ5min���N2O5ת����20%���ԣ�NO2��Ϊ______��5minʱ��N2O5ռ����������������______���Ķ����ϣ��ش�2������3��С��пͭԭ����û�ͼ�ķ�ʽ����ͼ����ʾ�ܲ����㣬�������õ��ͼʽ����ʽ����Zn|ZnSO4��1mol/L��||CuSO4��1mol/L��|Cu ��ʽ�У�����������Ӧ�ĸ���д����ߣ�������ԭ��Ӧ������д���ұߣ���ʵ���ߡ�|����ʾ�缫����Һ֮��Ľ��棬��˫ʵ���ߡ�||����ʾ���ţ�
��2�����������оٵĵ���У�пƬ�Ϸ����ĵ缫��Ӧʽ��______��
��3������һ��أ���ͼʽ����ʽΪCu|CuSO4��1mol/L��||Fe2��SO4��3��0.5mol/L��|C���õ���У������ĵ缫��Ӧʽ��______�������ĵ缫��Ӧʽ��______��
��4��д��֧��ֻ��һ���һ���ʽ����С�������Ľṹ��ʽ______��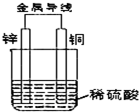
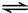
4NO2��g��+O2��g������Ӧ5min���N2O5ת����20%���ԣ�NO2��Ϊ______��5minʱ��N2O5ռ����������������______���Ķ����ϣ��ش�2������3��С��пͭԭ����û�ͼ�ķ�ʽ����ͼ����ʾ�ܲ����㣬�������õ��ͼʽ����ʽ����Zn|ZnSO4��1mol/L��||CuSO4��1mol/L��|Cu ��ʽ�У�����������Ӧ�ĸ���д����ߣ�������ԭ��Ӧ������д���ұߣ���ʵ���ߡ�|����ʾ�缫����Һ֮��Ľ��棬��˫ʵ���ߡ�||����ʾ���ţ�
��2�����������оٵĵ���У�пƬ�Ϸ����ĵ缫��Ӧʽ��______��
��3������һ��أ���ͼʽ����ʽΪCu|CuSO4��1mol/L��||Fe2��SO4��3��0.5mol/L��|C���õ���У������ĵ缫��Ӧʽ��______�������ĵ缫��Ӧʽ��______��
��4��д��֧��ֻ��һ���һ���ʽ����С�������Ľṹ��ʽ______��

��1��2N2O5��g��?4NO2��g��+O2��g����
2 4
��4��20%��mol 1.6mol
v��NO2��=
=
=0.16mol/��L?min��
����ͬ�����£�����������ʵ���֮�ȵ������֮�ȣ�
2N2O5��g��?4NO2��g��+O2��g�� ���������ӣ�
2 3
��4��20%��mol 1.2mol
���Ի����������ʵ���Ϊ4mol+1.2mol=5.2 mol��
���������N2O5�����ʵ���Ϊ��4-0.8��mol=3.2mol��
N2O5ռ�����������ʵ�������Ϊ
����00%=61.5%
�ʴ�Ϊ��0.16mol/��L?min����61.5%
��2�����ݵ缫���ϻ������жϣ�п��������пʧȥ���ӱ�����ӽ�����Һ������������Ӧ��
�ʴ�Ϊ��Zn-2e-=Zn2+
��3�����ݵ缫���ϻ������жϣ�ͭ��������̼��������ͭʧ���� ���ͭ���ӽ�����Һ������������Ӧ����Һ�����������ӵõ������ɶ��������ӣ�������ԭ��Ӧ��
�ʴ�Ϊ����+��2Fe3++2e-=2Fe2+����-��Cu-2e-=Cu2+
��4������֪ʶǨ�Ƶķ�����𣬸������൱�ڼ����е���ԭ�ӱ�����ȡ����������һ���������̼ԭ��������5�������Ը����൱�ڼ����е�3����ԭ�ӱ��һ�ȡ�����ʸ����Ľṹ��ʽ
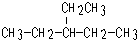
�ʴ�Ϊ
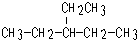
2 4
��4��20%��mol 1.6mol
v��NO2��=
| ��n |
| V��t |
| 1.6mol |
| 2L5min |
����ͬ�����£�����������ʵ���֮�ȵ������֮�ȣ�
2N2O5��g��?4NO2��g��+O2��g�� ���������ӣ�
2 3
��4��20%��mol 1.2mol
���Ի����������ʵ���Ϊ4mol+1.2mol=5.2 mol��
���������N2O5�����ʵ���Ϊ��4-0.8��mol=3.2mol��
N2O5ռ�����������ʵ�������Ϊ
| 3.2mol |
| 5.2mol |
�ʴ�Ϊ��0.16mol/��L?min����61.5%
��2�����ݵ缫���ϻ������жϣ�п��������пʧȥ���ӱ�����ӽ�����Һ������������Ӧ��
�ʴ�Ϊ��Zn-2e-=Zn2+
��3�����ݵ缫���ϻ������жϣ�ͭ��������̼��������ͭʧ���� ���ͭ���ӽ�����Һ������������Ӧ����Һ�����������ӵõ������ɶ��������ӣ�������ԭ��Ӧ��
�ʴ�Ϊ����+��2Fe3++2e-=2Fe2+����-��Cu-2e-=Cu2+
��4������֪ʶǨ�Ƶķ�����𣬸������൱�ڼ����е���ԭ�ӱ�����ȡ����������һ���������̼ԭ��������5�������Ը����൱�ڼ����е�3����ԭ�ӱ��һ�ȡ�����ʸ����Ľṹ��ʽ
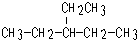
�ʴ�Ϊ
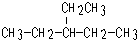

��ϰ��ϵ�д�
�����Ŀ
��Ӧ4NH3��g��+5O2��g��?4NO��g��+6H2O��g����2L�ĺ����ܱ������н��У�1min��NH3������0.12mol����ƽ��ÿ����Ũ�ȱ仯������ǣ�������
| A��NO��0.001 mol?L-1 | B��O2��0.00125 mol?L-1 | C��NH3��0.002 mol?L-1 | D��H2O��0.0015 mol?L-1 |
 ��2012?��ɫ��ģ����2L���ܱ�������Ͷ��һ����NO2��������Ӧ2NO2��g��?2NO��g��+O2��g�����ֱ���a��b���ֲ�ͬʵ�������·�Ӧ���ó�NO2��Ũ����ʱ��仯��������ͼ��ʾ��
��2012?��ɫ��ģ����2L���ܱ�������Ͷ��һ����NO2��������Ӧ2NO2��g��?2NO��g��+O2��g�����ֱ���a��b���ֲ�ͬʵ�������·�Ӧ���ó�NO2��Ũ����ʱ��仯��������ͼ��ʾ��