题目内容
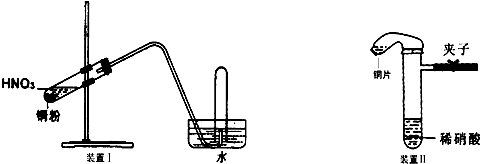
下图是化学研究性学习小组设计的铜与稀硝酸反应的两个实验装置图。其中装置Ⅰ为甲同学设计。

装置Ⅰ 装置Ⅱ
请回答下列问题:
(1)铜与稀硝酸反应的离子方程式为____________________________________________。
(2)乙同学认为装置Ⅰ中收集的气体不能确定铜与稀硝酸反应生成的是NO气体,理由是________________________________________________。于是他设计装置Ⅱ,其中装铜片的是气球。
(3)如何检验装置Ⅱ的气密性?
(4)化学研究性学习小组的其他同学对上述实验进行了研究,认为装置Ⅱ虽然作了改进,但如果按装置Ⅱ进行实验,还是会出现三个问题,需要作相应改进措施。请你帮助他们填写相关内容。
问题一:______________________________________________________________。
措施:加热或______________。
问题二:试管中的气体是淡棕红色,而不是无色。
措施:____________(填具体操作,不能增加装置)。
问题三:______________________________________________________________。
措施:________________________________________________________________。
(1)3Cu+8H++2![]()
![]() 3Cu2++2NO↑+4H2O
3Cu2++2NO↑+4H2O
(2)因为NO2与水反应也可产生NO:3NO2+H2O![]() 2HNO3+NO,故不能肯定生成的NO气体是来自于铜与稀硝酸反应
2HNO3+NO,故不能肯定生成的NO气体是来自于铜与稀硝酸反应
(3)关紧夹子,用酒精灯稍加热试管,气球鼓起,撤掉酒精灯后,气球恢复原貌,表明装置不漏气。(或其他合理答案 )
(4)问题一:反应速率较慢
措施:将铜片改为铜粉
问题二:
措施:先将少量碳酸盐倒入试管,然后迅速系上装有铜片的小气球
问题三:实验污染空气
措施:连接导管,将导管插入装有NaOH溶液的试管,并向试管中持续通入空气(其他合理答案也可)
解析:(2)因为NO2能与水反应生成NO,所以装置Ⅰ不能确定铜与稀硝酸反应生成的是NO气体。(3)关紧夹子,用酒精灯微热试管,气球鼓起,撤掉酒精灯后,气球恢复原状,表明装置不漏气。(4)铜片与稀硝酸在常温下反应较慢,可采取加热或把铜片改成铜粉的措施加快反应速率;试管中的气体呈淡棕红色,是因为未排除试管中的空气,可先将少量碳酸盐倒入试管,再迅速系上装有铜片的小气球;该实验缺少尾气处理装置,会污染空气,可连接导管,将导管插入装有NaOH溶液的试管,并向试管中持续通入空气。

(15分)硬质玻璃管是化学实验中经常使用的一种仪器,请分析下列实验(固定装置略)并回答问题。
Ⅰ、进行微量实验:如图所示,将浓硫酸滴入装有Na2SO3固体的培养皿一段时间后,a、b、c三个棉球变化如下表。请填写表中的空白:

|
棉球 |
棉球上滴加的试剂 |
实验现象 |
解释和结论 |
|
a |
|
棉球变白,微热后又恢复红色 |
|
|
b |
含酚酞的NaOH溶液 |
棉球变为白色 |
离子方程式: |
|
c |
|
棉球变为白色 |
该气体具有 (选填“氧化性”或“还原性”) |
Ⅱ、硬质玻璃管与其它装置结合完成定性或定量实验。下图是某研究性学习小组对某铁矿石中铁的氧化物的化学式进行探究的装置。

实验一:铁矿石中含氧量的测定
(1)按上图组装仪器(夹持仪器均省略),检查装置的气密性;
(2)将10.0g铁矿石放入硬质玻璃管中;
(3)从左端导气管口处不断地缓缓通入H2, 后,点燃A处酒精灯;
(4)充分反应后,撤掉酒精灯,再持续通入氢气至完全冷却。
(5)测得反应后装置B增重2.70g,则铁矿石中氧的质量分数为______________________。
实验二:铁矿石中含铁量的测定

(1)步骤②和⑤中都要用到的玻璃仪器是 __。
(2)下列有关步骤⑥的操作中说法不正确的是_______。
a.滴定管用蒸馏水洗涤后再用待装液润洗
b.锥形瓶需要用待测液润洗
c.因为碘水为黄色,所以滴定过程中不需加指示剂
实验结论:推算铁的氧化物的组成,由实验一、二得出该铁矿石中铁的氧化物的化学式为
硬质玻璃管是化学实验中经常使用的一种仪器,请分析下列实验(固定装置略)并回答问题。
Ⅰ、进行微量实验:如图所示,将浓硫酸滴入装有Na2SO3固体的培养皿一段时间后,a、b、c三个棉球变化如下表。请填写表中的空白:

|
棉球 |
棉球上滴加的试剂 |
实验现象 |
解释和结论 |
|
a |
|
棉球变白,微热后又恢复红色 |
|
|
b |
含酚酞的NaOH溶液 |
棉球变为白色 |
离子方程式:
|
|
c |
|
棉球变为白色 |
结论:该气体具有 性 |
Ⅱ、硬质玻璃管与其它装置结合完成定性或定量实验。下图是某研究性学习小组对某铁矿石中铁的氧化物的化学式进行探究的装置。

实验一:铁矿石中含氧量的测定
a.按上图组装仪器(夹持仪器均省略),检查装置的气密性;
b.将5.0g铁矿石放入硬质玻璃管中;
c.从左端导气管口处不断地缓缓通入H2, 后,点燃A处酒精灯;
d.充分反应后,撤掉酒精灯,再持续通入氢气至完全冷却。
(1)步骤c中填空
(2)测得反应后装置B增重1.35g,则铁矿石中氧的质量分数为______________________。实验二:铁矿石中含铁量的测定

(3)步骤④中煮沸的目的是_____________________________________________。
(4)步骤②和⑤中都要用到的玻璃仪器是______ __。
(5)下列有关步骤⑥的操作中说法不正确的是_______________________________。
a.滴定管用蒸馏水洗涤后再用待装液润洗
b.锥形瓶不需要用待测液润洗
c.因为碘水为黄色,所以滴定过程中不需加指示剂
实验结论:推算铁的氧化物的组成
(6)由实验一、二得出该铁矿石中铁的氧化物的化学式为____________________________。