题目内容
(2011?松江区模拟)2011年3月,日本福岛核电站发生核泄漏,核泄漏的放射性物质中,大量存在一种叫做“碘-131”的放射性元素.传说吃含碘食品或服碘片可以减缓碘-131对人体的影响,有些人就去抢购碘盐、碘片.下表是某食用碘盐包装袋上的部分说明:
(1)下列说法正确的是
A.碘酸钾可氧化氯化钠 B.只用淀粉就能检验碘盐中的碘酸钾 C.高温会导致碘的损失 D.该碘盐中碘酸钾含量约为34~84mg/kg
(2)碘酸钾在工业上可用电解法制取.以石墨和不锈钢为电极,以KI溶液为电解液,在一定条件下电解,反应的方程式为:KI+3H2O
KIO3+3H2↑.则阳极材料为
(3)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式.
该反应的氧化剂为
(4)已知:I2+2S2O32-→2I-+S4O62-.某学生测定食用碘盐中碘的含量,其步骤为:
a.准确称取w g食盐,加适量蒸馏水使其完全溶解 b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全 c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol?L-1的Na2S2O3溶液10.0mL,恰好反应完全.则所测盐中碘的含量是(以含w的代数式表示)
mg/kg.
| 配 料 | 食盐、碘酸钾、抗结剂 |
| 碘含量 | 35±15mg/kg |
| 储藏方法 | 密封、避光、防潮 |
| 食用方法 | 烹饪时,待食品熟后加入碘盐 |
CD
CD
A.碘酸钾可氧化氯化钠 B.只用淀粉就能检验碘盐中的碘酸钾 C.高温会导致碘的损失 D.该碘盐中碘酸钾含量约为34~84mg/kg
(2)碘酸钾在工业上可用电解法制取.以石墨和不锈钢为电极,以KI溶液为电解液,在一定条件下电解,反应的方程式为:KI+3H2O
| 电解 |
石墨
石墨
.(3)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式.
1
1
KIO3+5
5
KI+3
3
H2SO4→3
3
K2SO4+3
3
I2+3
3
H2O该反应的氧化剂为
KIO3
KIO3
(4)已知:I2+2S2O32-→2I-+S4O62-.某学生测定食用碘盐中碘的含量,其步骤为:
a.准确称取w g食盐,加适量蒸馏水使其完全溶解 b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全 c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol?L-1的Na2S2O3溶液10.0mL,恰好反应完全.则所测盐中碘的含量是(以含w的代数式表示)
| 423 |
| w |
| 423 |
| w |
分析:(1)根据食用碘盐的储存方法和食用方法推测可能具有的性质;
(2)电解时,阳极为惰性电极;
(3)根据氧化还原反应遵循电子守恒和质量守恒进行配平;
(4)根据反应的关系式:KIO3~3I2~6S2O32-,进行计算.
(2)电解时,阳极为惰性电极;
(3)根据氧化还原反应遵循电子守恒和质量守恒进行配平;
(4)根据反应的关系式:KIO3~3I2~6S2O32-,进行计算.
解答:解:(1)A.食盐中加入碘酸钾,说明二者可共存,能稳定存在,说明二者之间不发生反应,故A错误;
B.淀粉只能检验碘单质,与碘酸钾不反应,故B错误;
C.由“烹饪时,待食品熟后加入碘盐”知高温会导致碘的损失,故C正确;
D.由碘的含量35±15mg/kg,该碘盐中碘酸钾含量约为20×
~50×
,即34~84mg/kg,故D正确.
故答案为:CD;
(2)由电解方程式可知电解时KI在阳极被氧化,说明阳极为惰性电极材料,应为石墨,故答案为:石墨;
(3)反应中KIO3与KI之间发生氧化还原反应生成I2,根据氧化剂、还原剂之间得失电子数目相等可知KIO3~5KI,结合质量守恒可得:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O,其中KIO3为氧化剂,
故答案为:1;5;3;3;3;3;KIO3;
(4)反应的关系式为:KIO3~3I2~6S2O32-,n(Na2S2O3)=2.0×10-3mol?L-1×0.01L=2.0×10-5mol,
所以:n(KIO3)=
×n(Na2S2O3)=
×2.0×10-5mol,
m(I)=
×2.0×10-5mol×127g/mol=42.3×10-5g,
所以wkg食盐中含有42.3×10-5×106mg=423mg,
则所测盐中碘的含量是
mg/kg,
故答案为:
.
B.淀粉只能检验碘单质,与碘酸钾不反应,故B错误;
C.由“烹饪时,待食品熟后加入碘盐”知高温会导致碘的损失,故C正确;
D.由碘的含量35±15mg/kg,该碘盐中碘酸钾含量约为20×
| 214 |
| 127 |
| 214 |
| 127 |
故答案为:CD;
(2)由电解方程式可知电解时KI在阳极被氧化,说明阳极为惰性电极材料,应为石墨,故答案为:石墨;
(3)反应中KIO3与KI之间发生氧化还原反应生成I2,根据氧化剂、还原剂之间得失电子数目相等可知KIO3~5KI,结合质量守恒可得:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O,其中KIO3为氧化剂,
故答案为:1;5;3;3;3;3;KIO3;
(4)反应的关系式为:KIO3~3I2~6S2O32-,n(Na2S2O3)=2.0×10-3mol?L-1×0.01L=2.0×10-5mol,
所以:n(KIO3)=
| 1 |
| 6 |
| 1 |
| 6 |
m(I)=
| 1 |
| 6 |
所以wkg食盐中含有42.3×10-5×106mg=423mg,
则所测盐中碘的含量是
| 423 |
| w |
故答案为:
| 423 |
| w |
点评:本题考查较为综合,涉及元素化合物知识、氧化还原反应、电化学以及物质的含量测定,题目难度较大,本题注意计算中关系式的应用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

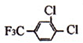 +
+
 +HCl
+HCl A发生缩聚反应
A发生缩聚反应 +nH2O
+nH2O 的含有三氟甲基(F3C一)和苯环的同分异构体共有
的含有三氟甲基(F3C一)和苯环的同分异构体共有