题目内容
(2011?松江区模拟)通常状况下,NC13是一种油状液体,其分子空间构型与氨分子相似,下列对NC13的有关叙述正确的是( )
分析:A、原子半径越小,原子间形成的键长越短.
B、如果元素的最外层电子数+元素的化合价的绝对值=8,该元素就达到8电子稳定结构,否则没有达到8电子稳定结构.
C、根据该分子是否是对称结构判断分子的极性.
D、物质的熔沸点越低越容易挥发.
B、如果元素的最外层电子数+元素的化合价的绝对值=8,该元素就达到8电子稳定结构,否则没有达到8电子稳定结构.
C、根据该分子是否是对称结构判断分子的极性.
D、物质的熔沸点越低越容易挥发.
解答:解:A、C原子的原子半径大于N原子的原子半径,所以CCl4中C-C1键键长比NC13中N-C1键键长,故A错误.
B、NC13中N原子最外层电子数5+化合价的绝对值3=8,所以N原子达到8电子稳定结构;NC13中C1原子最外层电子数7+化合价的绝对值1=8,所以C1原子达到8电子稳定结构,故B正确.
C、NC13的分子空间构型与氨分子相似,都是三角锥型结构,氨分子是极性分子,所以NCl3分子也是极性分子,故C错误.
D、分子晶体中物质的熔沸点与相对分子质量有关,相对分子质量越大其熔沸点越高,所以NBr3比NCl3的熔沸点高,NCl3比NBr3易挥发,故D错误.
故选B.
B、NC13中N原子最外层电子数5+化合价的绝对值3=8,所以N原子达到8电子稳定结构;NC13中C1原子最外层电子数7+化合价的绝对值1=8,所以C1原子达到8电子稳定结构,故B正确.
C、NC13的分子空间构型与氨分子相似,都是三角锥型结构,氨分子是极性分子,所以NCl3分子也是极性分子,故C错误.
D、分子晶体中物质的熔沸点与相对分子质量有关,相对分子质量越大其熔沸点越高,所以NBr3比NCl3的熔沸点高,NCl3比NBr3易挥发,故D错误.
故选B.
点评:明确熔沸点大小的判断方法、化合物中原子最外层电子数是否为8的判断方法、原子半径与键长的关系即可解答本题,难度不大.

练习册系列答案
相关题目

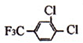 +
+
 +HCl
+HCl A发生缩聚反应
A发生缩聚反应 +nH2O
+nH2O 的含有三氟甲基(F3C一)和苯环的同分异构体共有
的含有三氟甲基(F3C一)和苯环的同分异构体共有