题目内容
 有A、B、C、D、E、F六种元素,A是周期表中原子半径最小的元素,B是电负性最大 的元素,C的2p轨道中有三个未成对的单电子,F原子核外电子数是B与C核外电子数之和,D是主族元素且与E同周期,E能形成红色(或砖红色)的E20和黑色的EO两种氧化物,D与B可形成离子化合物,其晶胞结构如右图所示.请回答下列问题.
有A、B、C、D、E、F六种元素,A是周期表中原子半径最小的元素,B是电负性最大 的元素,C的2p轨道中有三个未成对的单电子,F原子核外电子数是B与C核外电子数之和,D是主族元素且与E同周期,E能形成红色(或砖红色)的E20和黑色的EO两种氧化物,D与B可形成离子化合物,其晶胞结构如右图所示.请回答下列问题.
(1)E元素原子基态时的电子排布式为 .
(2)A2F分子中F原子的杂化类型是
(3)CA3极易溶于水,其原因主要是 ,
 (4)富勒烯衍生物由于具有良好的光电性能,在太阳能电池的应用上具有非常光明的前途.富勒烯(C60)的结构如右图,分子中碳原子轨道的杂化类型为 ;1 molC60分子中σ键的数目为 .
(4)富勒烯衍生物由于具有良好的光电性能,在太阳能电池的应用上具有非常光明的前途.富勒烯(C60)的结构如右图,分子中碳原子轨道的杂化类型为 ;1 molC60分子中σ键的数目为 .
(5)多元化合物薄膜太阳能电池材料为无机盐,其主要包括
砷化镓、硫化镉、硫化锌及铜铟硒薄膜电池等.
①第一电离能:As Se(填“>”“<”或“=”).
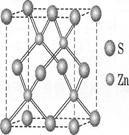
②硫化锌的晶胞中(结构如下图所示),硫离子的配位数
是 与S距离最近且等距离的S之间的距离为
(密度为ρg/cm3)
③二氧化硒分子的空间构型为 .
![]() (2分)
(2分)
(2)SP3 (1分)、
(3)与水分子之间形成氢键 (2分)
(4) ![]() ( 前一个1分),(后一个2分)
( 前一个1分),(后一个2分)
(5) ![]()
![]() (每空2分)③
(每空2分)③![]() (1分)
(1分)

练习册系列答案
相关题目





