题目内容
元素之间通过不同的化学键可以组成不同的晶体和化合物.有关化学键与晶体的说法正确的是( )
| A、两种元素组成的分子中一定只有极性键 | B、熔融状态时能导电的化合物一定是离子晶体 | C、非金属元素组成的化合物一定是共价化合物 | D、分子晶体的熔沸点随着共价键的增强而升高 |
分析:A.H2O2中既含有极性键又含有非极性键;
B.熔融状态能导电的化合物一定是离子化合物;
C.由非金属元素组成的化合物可能为离子化合物,如铵盐;
D.分子晶体熔沸点取决于分子间作用力与化学键无关.
B.熔融状态能导电的化合物一定是离子化合物;
C.由非金属元素组成的化合物可能为离子化合物,如铵盐;
D.分子晶体熔沸点取决于分子间作用力与化学键无关.
解答:解:A.两种元素组成的分子中不一定只有极性键,如.H2O2中既含有极性键又含有非极性键,故A错误;
B.熔融状态能导电的化合物是离子化合物,说明该化合物中含有自由移动的离子,故B正确;
C.由非金属元素组成的化合物可能为离子化合物,如铵盐,所以由非金属元素组成的化合物不一定是共价化合物,故C错误;
D.分子晶体熔沸点取决于分子间作用力与化学键无关,故D错误;
故选B.
B.熔融状态能导电的化合物是离子化合物,说明该化合物中含有自由移动的离子,故B正确;
C.由非金属元素组成的化合物可能为离子化合物,如铵盐,所以由非金属元素组成的化合物不一定是共价化合物,故C错误;
D.分子晶体熔沸点取决于分子间作用力与化学键无关,故D错误;
故选B.
点评:本题考查了本题考查了键的极性、离子化合物与共价化合物判断、分子晶体熔沸点规律,注意分子晶体沸点规律.

练习册系列答案
相关题目
[化学--物质结构与性质]
四种常见元素:A、B、C、D为周期表前四周期元素,原子序数依次递增,它们的性质或结构信息如下表.试根据信息回答有关问题.
(1)写出D原子的外围电子排布式______,A、B、C、D四种元素的第一电离能最小的是______(用元素符号表示).
(2)B元素的氢化物的沸点比同主族相邻元素氢化物沸点______(填“高”或“低”).
(3)元素F与A相邻且同主族,它们与氧元素的成键情况如下:
在A和O之间通过双键形成AO2分子,而F和O则不能和A那样形成有限分子,原因是______.
(4)往D元素的硫酸盐溶液中逐滴加入过量B元素的氢化物水溶液,可生成的配合物,该配合物中不含有的化学键是______(填序号).a.离子键 b.极性键c.非极性键d.配位键 e.金属键
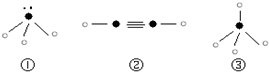
(5)下列分子结构图中的“ ”表示上述相关元素的原子中除去最外层电子的剩余部分,“
”表示上述相关元素的原子中除去最外层电子的剩余部分,“ ”表示氢原子,小黑点“
”表示氢原子,小黑点“ ”表示没有形成共价键的最外层电子,短线表示共价键.
”表示没有形成共价键的最外层电子,短线表示共价键.

则在以上分子中,中心原子采用sp3杂化形成化学键的是______(填序号);在②的分子中有______个σ键和______个π键.
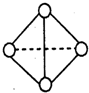
(6)已知一种分子B4分子结构如图所示,断裂1molB-B吸收aKJ的热量,生成1molB≡B放出bKJ热量.试计算反应:B4(g)═2B2(g)△H=______KJ/mol.

四种常见元素:A、B、C、D为周期表前四周期元素,原子序数依次递增,它们的性质或结构信息如下表.试根据信息回答有关问题.
| 元素 | A | B | C | D |
| 结构性质 信息 | 基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子数相同 | 原子核外有两个电子层,最外层有3个未成对的电子 | 基态原子的M层有2对成对的p电子 | 其原子序数比A、B、C三种元素原子的质子数总和还少1,有+1、+2两种常见化合价 |
(2)B元素的氢化物的沸点比同主族相邻元素氢化物沸点______(填“高”或“低”).
(3)元素F与A相邻且同主族,它们与氧元素的成键情况如下:
| A-O | A=O | F-O | F=O | |
| 键能(KJ/mol) | 360 | 803 | 464 | 640 |
(4)往D元素的硫酸盐溶液中逐滴加入过量B元素的氢化物水溶液,可生成的配合物,该配合物中不含有的化学键是______(填序号).a.离子键 b.极性键c.非极性键d.配位键 e.金属键
(5)下列分子结构图中的“
 ”表示上述相关元素的原子中除去最外层电子的剩余部分,“
”表示上述相关元素的原子中除去最外层电子的剩余部分,“ ”表示氢原子,小黑点“
”表示氢原子,小黑点“ ”表示没有形成共价键的最外层电子,短线表示共价键.
”表示没有形成共价键的最外层电子,短线表示共价键.
则在以上分子中,中心原子采用sp3杂化形成化学键的是______(填序号);在②的分子中有______个σ键和______个π键.
(6)已知一种分子B4分子结构如图所示,断裂1molB-B吸收aKJ的热量,生成1molB≡B放出bKJ热量.试计算反应:B4(g)═2B2(g)△H=______KJ/mol.

 ”表示上述相关元素的原子中除去最外层电子的剩余部分,“
”表示上述相关元素的原子中除去最外层电子的剩余部分,“ ”表示氢原子,小黑点“
”表示氢原子,小黑点“

 尿素(
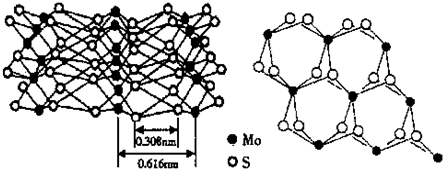
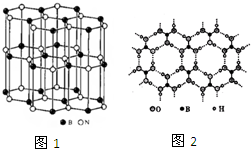
尿素(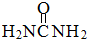 )和硼砂(Na2B4O7)在高温高压下反应可以获得硼氮化合物:
)和硼砂(Na2B4O7)在高温高压下反应可以获得硼氮化合物: