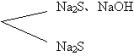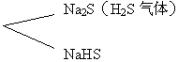题目内容
往400mL0.5 mol•L-1的NaOH溶液中通人一定量的H2S气体,然后在低温条件下蒸干溶液,得到白色固体A为9.5g,
试问(1)分析推断出白色固体A可能有的组成。(2)通过计算确定白色固体A的组成及各物质的质量。
解析:
H2S气体通入NaOH溶液中发生了酸碱中和反应,因为氢硫酸为二元酸在与NaOH溶液反应时,将有两种可能发生的反应,即:①H2S + 2NaOH = Na2S + 2H2O; ②H2S + NaOH = NaHS + H2O 随着 当 当 当 再按照题给白色固体A为9.5 g,通过计算确定它符合上述哪一种情况后,再解出它们的质量。 计算推断: 按①式 H2S + 2NaOH = Na2S + 2H2O 2 1 0.5×0.004 x 得 按②式 H2S + NaOH = NaHS + H2O 1 1 0.5×0.400 y 得NaHS y=0.5×0.400=0.2mol 即得白色固体A的质量为0.2×56=11.2 g,11.2 g>9.5 g 由此可见白色固体A应由Na2S和NaHS组成。 各自质量求解如下:设①式NaOH需用x mol ① H2S + 2NaOH = Na2S + 2H2O 2 1 x ② H2S + NaOH = NaHS + H2O 1 1 0.5×0.400-x 0.5×0.400-x ∴ NaHS为0.2-x mol质量为0.1×56=5.6 g
|

 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案