题目内容
用NA表示阿伏加德罗常数,下列叙述正确的是 ( )
| A.2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA |
| B.0.5molC3H8分子中所含C-H共价键数为2NA |
| C.标准状况下,22.4L乙醇完全燃烧所耗的氧气分子数为3NA |
D.1mol碳正离子 所含的电子数为11NA 所含的电子数为11NA |
A
解析试题分析:A、乙烯和丙烯的最简式均是CH2,2.8g的混合气体中含0.2mol的CH2,所以C原子数为0.2NA,正确;B、0.5molC3H8分子中所含C-H共价键数为0.5mol×8=4NA,错误;C、标准状况下,乙醇不为气体,所以物质的量无法计算,耗氧量无法计算,错误;D、1mol碳正离子 所含的电子数为10NA,错误,答案选A。
所含的电子数为10NA,错误,答案选A。
考点:考查对阿伏伽德罗常数的理解应用

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
NA为阿伏伽德罗常数。下列说法正确的是( )
| A.同温同压同体积的CO2和SO2所含氧原子数均为2NA |
| B.32gCu与S完全反应转移的电子数为NA |
| C.1L 1.0mol·L-1NH4Cl与2L 0.5mol·L-1NH4Cl溶液含NH4+数目相同 |
| D.25℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH-数目为0.1NA |
设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.标况下,11.2L乙烷中含有共价键的数目为3NA |
| B.标况下,22.4LO2和CO2组成的混合物中含有氧原子数为2NA |
| C.常温下,22.4L甲烷中含有的电子数为10NA |
| D.常温下,1 L 0.1mol·L-1的Na2CO3溶液中含OH-离子数为0.1NA |
设NA为阿伏加德罗常数的值。下列叙述正确的是
| A.1 L 1 mol·L-1的NaClO 溶液中含有ClO-的数目为NA |
| B.pH=1的醋酸溶液中,CH3COO-和OH-数目之和为0.1NA |
| C.78 g苯中含有碳碳双键的数目为3NA |
| D.标准状况下,6.72 L NO2与水充分反应转移的电子数目为0.2NA |
设NA为阿伏伽德罗常数的值。下列说法正确的是
| A.标准状况下,0.1molCl2溶于水,转移的电子数目为0.1NA |
| B.常温常压下,18g H2O含有的原子总数为3NA |
| C.标准状况下,11.2LCH3CH2OH中含有分子的数目为0.5NA |
| D.常温常压下,2.24LCO和CO2混合气体中含有的碳原子数目为0.1NA |
用NA表示阿伏加德罗常数,下列结论能够成立的是
| A.0.1 mol·L-1的Na2CO3溶液中含有CO32-的个数是小于0.1NA |
| B.1 molFe与足量稀硝酸完全反应转移的电子数为2NA |
| C.0.2mol·L-1 CuSO4溶液加水稀释至体积增加1倍,其浓度变为0.1 mol·L-1 |
| D.4g NaOH固体溶解1L水中,所得溶液的物质的量浓度为0.1mol/L |
下列说法中正确的是
| A.6.8 g熔融KHSO4与3.9 g熔融Na2O2中阴离子数目相同 |
B.某金属阳离子的结构示意图为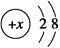 ,其与Cl-形成的强电解质都是离子化合物 ,其与Cl-形成的强电解质都是离子化合物 |
C.二硫化碳是直线形非极性分子,其电子式为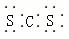 |
| D.中子数为18的氯原子可表示为18Cl |
下列叙述正确的是 ( )。
| A.1 L 0.1 mol·L-1碳酸钠溶液的阴离子总数等于0.1NA |
| B.将1体积c mol·L-1硫酸用水稀释为5体积,得到0.2c mol·L-1硫酸 |
| C.将25 g无水CuSO4溶于水制成100 mL溶液,其浓度为1 mol·L-1 |
D.将w g a%NaCl溶液蒸发掉 g水,得到4a% NaCl溶液 g水,得到4a% NaCl溶液 |