题目内容
氢镍电池是近年开发出来的可充电电池,可取代会产生镉污染的镉镍电池.氢镍电池的总反应为
H2+NiO(OH)
Ni(OH)2,据此反应判断,下列叙述中正确的是( )
| 1 |
| 2 |
| 放电 |
| 充电 |
| A、电池充电时,Ni(OH)2只作为阴极上反应的原料 |
| B、该反应属于可逆反应 |
| C、电池充电时,氢元素被还原 |
| D、电池放电时,H2是负极 |
考点:化学电源新型电池
专题:
分析:氢镍电池的总反应式是:
H2+NiO(OH)
Ni(OH)2,放电时,负极反应为:H2-2e-+2OH-=2H2O,正极反应为:NiO(OH)+H2O+e-=OH-+Ni(OH)2,充电时的电极反应为放电时的逆反应.
| 1 |
| 2 |
| 放电 |
| 充电 |
解答:
解:A.充电时,阴极反应为:2H2O+2e-=H2+2OH-,则Ni(OH)2不是阴极上反应的原料,故A错误;
B.原电池是自发的氧化还原反应,电解时是有外接电源的氧化还原反应,反应条件不同,不是可逆反应,故B错误;
C.充电时,阴极反应为,2H2O+2e-=H2+2OH-,氢元素被还原,故C正确;
D.电池放电时,负极反应为H2-2e-+2OH-=2H2O,则H2是负极,故D正确.
故选CD.
B.原电池是自发的氧化还原反应,电解时是有外接电源的氧化还原反应,反应条件不同,不是可逆反应,故B错误;
C.充电时,阴极反应为,2H2O+2e-=H2+2OH-,氢元素被还原,故C正确;
D.电池放电时,负极反应为H2-2e-+2OH-=2H2O,则H2是负极,故D正确.
故选CD.
点评:本题考查化学电源新型电池,题目难度不大,注意把握正负极的判断和电极反应式的书写,侧重于原电池原理的应用的考查.

练习册系列答案
相关题目
下列物质分类正确的是( )
A、 芳香族化合物 芳香族化合物 |
B、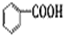 羧酸 羧酸 |
C、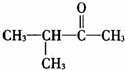 醛 醛 |
D、 酚 酚 |
下列有关物质的性质和该性质的应用均正确的是( )
| A、Na2O2是碱性氧化物,能与CO2、H2O反应作供氧剂 |
| B、浓硫酸具有强氧化性,常温下可用铝罐盛装 |
| C、SO2利Cl2均具有漂白性,两者混合使用可以增强漂白效果 |
| D、氯气具有酸性,可与烧碱或石灰乳反应制取含氯消毒剂 |
下列分子或离子在指定条件的分散系中能大量共存的是( )
| A、Ca(NO3)2溶液中:Fe2+、H+、Cl-、SO42- |
| B、使pH试纸变蓝的溶液中:K+、NH4+、S-、SO32- |
| C、水电离出的c(H+)=10-12 mol?L-1的溶液中:Na+、Ba2+、HCO3-、CH3COO- |
| D、透明的强酸性溶液中:Al3+、Fe3+、Cl-、SO42 |
下列反应不属于氧化还原反应的是( )
| A、锌放入稀硫酸中 |
| B、高锰酸钾分解 |
| C、实验室制备氨气 |
| D、碳和水蒸气在高温下反应 |
下列有关叙述中正确的是( )
| A、因为s轨道的形状是球形的,所以s电子做的是圆周运动 |
| B、3px、3py、3pz的差异之处在于三者中电子(基态)的能量不同 |
| C、原子轨道和电子云都是用来形象地描述电子运动状态的 |
| D、H2、F2、HCl和H2O中的σ键都是sp σ键 |
下列物质容易导电的是( )
| A、熔融状态下的氯化钾 | B、铜 |
| C、硫酸铜晶体 | D、无水乙醇 |