题目内容
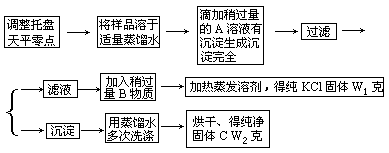
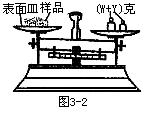
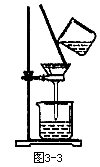
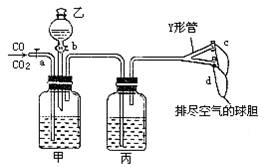
(1)灼热的CuO (2)饱和NaHCO3浓H2SO4 (3)将样品溶解在HCl(aq)中,然后过滤、洗涤 (4)将样品溶解在水中,然后过滤、洗涤 (5)向样品中加过量HCl(aq),逸出气体证明含CaCO3,有不溶物证明含SiO2
除杂时要根据杂质与主体物质的性质不同来选择试剂,同时不能引入新的杂质。除去CO2中的CO,可用灼热的氧化铜。除去CO2中的少量SO2,不能用碱溶液,或Na2CO3溶液,因为它们都能吸收CO2:2NaOH+CO2══Na2CO3+H2O,NaOH+CO2══NaHCO3;Na2CO3+H2O+CO2══2NaHCO3。SiO2与盐酸不反应,CaCO3可与盐酸反应生成CaCl2(aq)、CO2和水,然后将SiO2过滤出来。SiO2不溶于水,Na2SiO3能溶于水,可加水过滤将Na2SiO3除去。生石灰是CaO,属碱性氧化物,与酸反应生成盐和水,石英不溶于酸,石灰石溶于盐酸生成CaCl2、CO2和水。

练习册系列答案
相关题目