题目内容
2. 铁、铜及其化合物在日常生产、生活中有着广泛的应用.回答下列问题:
铁、铜及其化合物在日常生产、生活中有着广泛的应用.回答下列问题:(1)铁元素在周期表中的位置是第4周期VIII族,基态Cu2+的核外电子排布式是[Ar]3d9.元素铁与铜的第二电离能分别为:ICu=1958KJ•mol-1、IFe=1561KJ•mol-1,ICu>IFe的原因是铜失去1个电子后为3d10,轨道为全充满,相对较稳定,再失去电子较难;而铁失去1个电子后为3d64s1,再失去电子相对较易.
(2)有机铁肥三硝酸六尿素合铁(Ⅲ),化学式为:[Fe(H2NCONH2)6](NO3)3.
①尿素分子中C原子的杂化方式是sp2.
②[Fe(H2NCONH2)6](NO3)3 中“H2NCONH2”与 Fe(Ⅲ)之间的作用力是配位键.根据价层电子对互斥理论推测 NO3-的空间构型为平面三角形.
(3)Fe3+可用SCN-检验,其对应的酸有两种,分别为硫氰酸(H-S-C≡N)和异硫氰酸(H-N=C=S),这两种酸中沸点较高的是异硫氰酸(H-N=C=S),原因是异硫氰酸更易形成分子间氢键.
(4)FeCl3晶体易溶于水和乙醇,用酒精灯加热即可气化,由此可知 FeCl3的晶体类型为分子晶体;S和Fe形成的某化合物,其晶胞如图一所示,则该物质的化学式为FeS.
(5)Cu晶体的堆积方式如图二所示,晶体中Cu原子的配位数为12;设Cu原子半径为a,晶体空间利用率为$\frac{4×\frac{4}{3}π{a}^{3}}{(2\sqrt{2}×a)^{3}}×100%$(用含a 的式子表达,不化简).
分析 (1)铁元素在周期表中的位置是第4周期VIII族,基态Cu2+的核外电子排布式是[Ar]3d9,Fe的价电子排布式为[Ar]3d64s2,Cu的价电子排布式为[Ar]3d104s1,Cu失去一个电子后是3d能级全满,比较稳定,此时失去第二个电子不容易,据此分析原因;
(2)①尿素分子中C形成的是羰基,是一个平面型的基团,据此判断C的杂化方式;
②[Fe(H2NCONH2)6](NO3)3 是一个配合物,中心Fe(III)提供空轨道,则H2NCONH2是配体,提供孤电子对,形成配位键,根据VSEPR理论和杂化轨道理论判断NO3-的空间构型;
(3)比较硫氰酸(H-S-C≡N)和异硫氰酸(H-N=C=S),考虑分子间形成氢键对二者沸点的影响,据此分析原因;
(4)FeCl3晶体易溶于水和乙醇,用酒精灯加热即可气化,可判断FeCl3晶体是分子晶体,熔沸点较低,立方晶胞中,顶点粒子占$\frac{1}{8}$,面心粒子占$\frac{1}{2}$,晶胞内部粒子为整个晶胞所有,据此计算化学式;
(5)以最上层中心的Cu为参考点,与之接触的硬球有3层,每层有4个与之等径且最近,因此晶体中Cu的配位数为4×3=12,晶体的空间利用率=$\frac{{V}_{球}}{{V}_{晶胞}}×100%$,据此计算.
解答 解:(1)铁元素在周期表中的位置是第4周期VIII族,基态Cu2+的核外电子排布式是[Ar]3d9,
Fe的价电子排布式为[Ar]3d64s2,Cu的价电子排布式为[Ar]3d104s1,Cu失去一个电子后是3d能级全满,比较稳定,此时失去第二个电子不容易,因此ICu>IFe的原因是:铜失去1个电子后为3d10,轨道为全充满,相对较稳定,再失去电子较难;而铁失去1个电子后为3d64s1,再失去电子相对较易,
故答案为:第4周期VIII族;[Ar]3d9;铜失去1个电子后为3d10,轨道为全充满,相对较稳定,再失去电子较难;而铁失去1个电子后为3d64s1;再失去电子相对较易;
(2))①尿素分子中C形成的是羰基,是一个平面型的基团,因此C的杂化方式为sp2,
故答案为:sp2;
②[Fe(H2NCONH2)6](NO3)3 是一个配合物,中心Fe(III)提供空轨道,则H2NCONH2是配体,提供孤电子对,形成配位键,则H2NCONH2与 Fe(Ⅲ)之间的作用力是配位键,
对于NO3-,根据VSEPR理论,配位原子数为BP=3,孤电子对数为LP$\frac{5-2×3+1}{2}$=0,则其价电子对数为VP=BP+LP=3+0=3,根据杂化轨道理论,中心N原子为sp2杂化,空间构型为平面三角形,
故答案为:配位键;平面三角形;
(3)硫氰酸(H-S-C≡N)和异硫氰酸(H-N=C=S),H-S-C≡N中H和S相连,H-N=C=S中H和氮相连,N的电负性大于S,因此H-N=C=S中的H更具活性,能形成分子间氢键,导致其沸点升高,因此硫氰酸(H-S-C≡N)和异硫氰酸(H-N=C=S)这两种酸中沸点较高的是异硫氰酸(H-N=C=S),原因是:异硫氰酸更易形成分子间氢键,
故答案为:异硫氰酸(H-N=C=S);异硫氰酸更易形成分子间氢键;
(4)FeCl3晶体易溶于水和乙醇,用酒精灯加热即可气化,可判断FeCl3晶体是分子晶体,熔沸点较低,根据晶胞分析,立方晶胞中,顶点粒子占$\frac{1}{8}$,面心粒子占$\frac{1}{2}$,晶胞内部粒子为整个晶胞所有,因此一个晶胞中,含有Fe的个数为4,含有S的个数为$8×\frac{1}{8}+6×\frac{1}{2}$=4,则则该物质的化学式为:FeS,
故答案为:分子晶体;FeS;
(5)以最上层中心的Cu为参考点,与之接触的硬球有3层,每层有4个与之等径且最近,因此晶体中Cu的配位数为4×3=12,
根据Cu的晶胞结构,该晶胞中Cu的堆积方式为fcc,即面心立方最密堆积,能看出这个堆积方式,就不难知道配位数为12,对于面心立方最密堆积的晶胞而言,一个晶胞中含有的粒子个数为$8×\frac{1}{8}+6×\frac{1}{2}=4$,Cu原子半径为a,则晶胞内硬球的体积总和为V球=$4×\frac{4}{3}π{a}^{3}$,根据面心立方最密堆积的硬球接触模型,设晶胞参数为b,根据立体几何知识,存在关系:$\sqrt{2}b=4a$,则b=2$\sqrt{2}$a,因此晶胞的体积为V晶胞=(2$\sqrt{2}$a)3,所以,晶胞的空间利用率=$\frac{{V}_{球}}{{V}_{晶胞}}×100%$=$\frac{4×\frac{4}{3}π{a}^{3}}{(2\sqrt{2}×a)^{3}}×100%$,这就是答案,
如果接着算下去,则空间利用率=$\frac{4×\frac{4}{3}π}{(2\sqrt{2})^{3}}×100%$=74.05%,这就是面心立方最密堆积(fcc)的空间利用率!
故答案为:12;$\frac{4×\frac{4}{3}π{a}^{3}}{(2\sqrt{2}×a)^{3}}×100%$.
点评 本题考查物质结构知识,包含价电子排布式,电离能的比较,杂化轨道理论,价层电子对互斥理论,氢键的知识,晶胞的计算.题目涉及的知识点较多,考查综合能力,题目难度中等.

| A. | 氯化硼液态时能导电而固态时不导电 | |
| B. | 氯化硼中心原子采用sp杂化 | |
| C. | 氯化硼分子与氯化铝分子互为等电子体,都是非极性分子 | |
| D. | 氯化硼的熔沸点与氯硼键的键能大小有关 |
| A. | 22.4L O2的物质的量约为1mol | |
| B. | 标准状况下,11.2L H2O的物质的量约为1mol | |
| C. | 1mol/L的CuSO4溶液中SO42-的物质的量为1mol | |
| D. | 4.4g CO2含有的原子数为0.3NA |

| A. | 太阳能、风能、潮汐能 | B. | 水能、生物质能、天然气 | ||
| C. | 煤炭、生物质能、沼气 | D. | 地热能、石油、核能 |
| A. | 3v正(H2)=v逆(CH3OH) | B. | 混合气体的密度不再改变 | ||
| C. | 容器内压强不再改变 | D. | 反应物与生成物的浓度相等 |
| A. | 形成化学键 | B. | 氯化铵与氢氧化钡晶体混合 | ||
| C. | 铝热反应 | D. | 生石灰溶于水 |
 常温下,用0.05mol/LNaOH溶液分别滴定10.00mL浓度均为0.10mol/LCH3COOH( Ka=l×10-5)溶液HCN(Ka=5×10-10)溶液,所得滴定曲线如图.下列说法正确的是( )
常温下,用0.05mol/LNaOH溶液分别滴定10.00mL浓度均为0.10mol/LCH3COOH( Ka=l×10-5)溶液HCN(Ka=5×10-10)溶液,所得滴定曲线如图.下列说法正确的是( )| A. | 对两种弱酸滴定均可选用甲基橙作指示剂 | |
| B. | ③处溶液有:c(Na+)=c(CH3COO-)<c(CH3COOH) | |
| C. | 溶液中水的电离程度:②>③>④ | |
| D. | 点①和点②溶液混合后:c(CH3COO-)-c(CN-)=c(HCN)-c(CH3COOH) |
 某有机物由C、H、O三种元素组成,球棍模型如图所示:
某有机物由C、H、O三种元素组成,球棍模型如图所示: .
.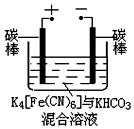 材料一:连二亚硫酸钠(Na2S2O4)是一种常用还原剂,俗称保险粉.工业制备方法如下:
材料一:连二亚硫酸钠(Na2S2O4)是一种常用还原剂,俗称保险粉.工业制备方法如下: