题目内容
 右图是反应CO(g)+2H2(g)
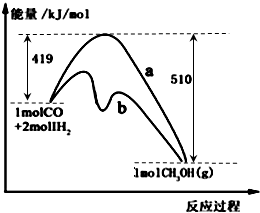
右图是反应CO(g)+2H2(g) CH3OH(g)进行过程中的能量变化曲线.曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化.下列相关说法正确的是( )
CH3OH(g)进行过程中的能量变化曲线.曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化.下列相关说法正确的是( )分析:A、依据催化剂只改变速率不改变平衡分析判断;
B、依据盖斯定律的内容,反应的焓变只与起始和终了状态有关,与变化过程无关;
C、依据图象中反应物和生成物能量的大小,结合拆化学键吸收能量,形成化学键放出能量分析判断;
D、依据图象中的能量变化,结合书写热化学方程式的要求写出.
B、依据盖斯定律的内容,反应的焓变只与起始和终了状态有关,与变化过程无关;
C、依据图象中反应物和生成物能量的大小,结合拆化学键吸收能量,形成化学键放出能量分析判断;
D、依据图象中的能量变化,结合书写热化学方程式的要求写出.
解答:解:A、曲线b表示使用催化剂后的能量变化,催化剂只改变所以速率,不改变化学平衡,所以反应物的转化率和生成物的产率不变,故A错误;
B、曲线a、b线进行的反应,b线使用催化剂降低了反应的活化能,改变了反应速率,但平衡开始和终了的物质能量未变,所以反应的热效应相同,故B正确;
C、图象中表示该反应是放热反应,所以拆化学键吸收的能量小于形成化学键所放出的能量,因此(1molCO+2molH2)中的键能之和比1molCH3OH中的键能之和小,故C错误;
D、图象中表示的是1molCO气体和2mol氢气反应生成1mol气态甲醇的反应热效应,反应放出热量=510KJ-419KJ=91KJ,根据热化学方程式的书写原则热化学方程式为:CO(g)+2H2(g) CH3OH(g)△H=-91kJ?mol-1,故D正确;
CH3OH(g)△H=-91kJ?mol-1,故D正确;
故选BD.
B、曲线a、b线进行的反应,b线使用催化剂降低了反应的活化能,改变了反应速率,但平衡开始和终了的物质能量未变,所以反应的热效应相同,故B正确;
C、图象中表示该反应是放热反应,所以拆化学键吸收的能量小于形成化学键所放出的能量,因此(1molCO+2molH2)中的键能之和比1molCH3OH中的键能之和小,故C错误;
D、图象中表示的是1molCO气体和2mol氢气反应生成1mol气态甲醇的反应热效应,反应放出热量=510KJ-419KJ=91KJ,根据热化学方程式的书写原则热化学方程式为:CO(g)+2H2(g)
 CH3OH(g)△H=-91kJ?mol-1,故D正确;
CH3OH(g)△H=-91kJ?mol-1,故D正确;故选BD.
点评:本题考查了化学反应中的能量变化形式和化学平衡的影响因素催化剂的作用,热化学方程式的书写,关键是理解图象的含义是解题的根本.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
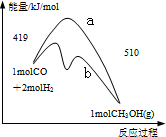
 氮氧化物是大气污染物之一,消除氮氧化物的方法有多种.
氮氧化物是大气污染物之一,消除氮氧化物的方法有多种.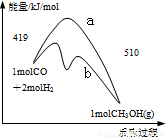
 CH3OH(g)进行过程中的能量变化曲线.曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化.下列相关说法正确的是( )
CH3OH(g)进行过程中的能量变化曲线.曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化.下列相关说法正确的是( )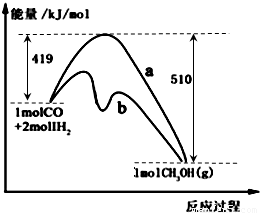
 CH3OH(g)△H=-91kJ?mol-1
CH3OH(g)△H=-91kJ?mol-1