题目内容
下列反应的离子方程式正确的是( )
| A、碳酸钠溶液显碱性:CO32-+2H2O?H2CO3+2OH - |
| B、氯气和水反应:Cl2+H2O=2H++Cl-+ClO- |
| C、用小苏打治疗胃酸过多:HCO3-+H+=CO2↑+H2O |
| D、氨气通入醋酸溶液中:NH3+H+=NH4+ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.碳酸根离子的水解分步进行,主要以第一步为主,其水解的离子方程式需要分别书写;
B.次氯酸为弱电解质,离子方程式中次氯酸不能拆开,应该保留分子式;
C.小苏打为碳酸氢钠,碳酸氢根离子与氢离子反应生成二氧化碳和水;
D.一水合氨和醋酸都是弱电解质,离子方程式中二者都应该保留分子式.
B.次氯酸为弱电解质,离子方程式中次氯酸不能拆开,应该保留分子式;
C.小苏打为碳酸氢钠,碳酸氢根离子与氢离子反应生成二氧化碳和水;
D.一水合氨和醋酸都是弱电解质,离子方程式中二者都应该保留分子式.
解答:
解:A.碳酸钠溶液中,碳酸根离子水解,溶液显示碱性,其水解过程需要局部进行,主要写出第一步的水解即可,正确的离子方程式为:CO32-+H2O?HCO3-+OH-,故A错误;
B.氯气和水反应生成氯化氢和次氯酸,次氯酸应该保留分子式,正确的离子方程式为:Cl2+H2O=H++Cl-+HClO,故B错误;
C.用小苏打治疗胃酸过多,实质为碳酸氢根离子与氢离子反应生成二氧化碳气体和水,反应的离子方程式为:HCO3-+H+=CO2↑+H2O,故C正确;
D.氨气通入醋酸溶液中,醋酸为弱酸,离子方程式中醋酸应该保留分子式,正确的离子方程式为:NH3+CH3COOH=NH4++CH3COO-,故D错误;
故选C.
B.氯气和水反应生成氯化氢和次氯酸,次氯酸应该保留分子式,正确的离子方程式为:Cl2+H2O=H++Cl-+HClO,故B错误;
C.用小苏打治疗胃酸过多,实质为碳酸氢根离子与氢离子反应生成二氧化碳气体和水,反应的离子方程式为:HCO3-+H+=CO2↑+H2O,故C正确;
D.氨气通入醋酸溶液中,醋酸为弱酸,离子方程式中醋酸应该保留分子式,正确的离子方程式为:NH3+CH3COOH=NH4++CH3COO-,故D错误;
故选C.
点评:本题考查了离子方程式的正误判断,为高考中的高频题,属于中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.

练习册系列答案
相关题目
下列说法正确的是( )
| A、用湿润的PH试纸可测溶液的酸碱性 |
| B、用碱式滴定管可量取5.00mLKMnO4溶液 |
| C、碳酸钠溶液可盛放于玻璃瓶塞的试剂瓶内 |
| D、氯水可用棕色试剂瓶保存于阴暗处 |
过量的某饱和一元醇14g与乙酸反应生成15.8g乙酸某酯,反应后可以回收该醇2.4g,饱和一元醇的相对分子质量约为( )
| A、98 | B、116 |
| C、188 | D、196 |
如图的装置能构成原电池并产生较强的电流的是( )
A、 |
B、 |
C、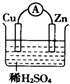 |
D、 |
已知G、Q、X、Y、Z均为含氯元素的化合物,在一定条件下有下列转化关系(未配平):
①G→Q+NaCl
②Q+H2O
X+H2
③Y+NaOH-→G+Q+H2O
④Z+NaOH-→Q+X+H2O
这五种化合物中Cl元素化合价由低到高的顺序是( )
①G→Q+NaCl
②Q+H2O
| ||
③Y+NaOH-→G+Q+H2O
④Z+NaOH-→Q+X+H2O
这五种化合物中Cl元素化合价由低到高的顺序是( )
| A、G、Y、Q、Z、X |
| B、X、Z、Q、G、Y |
| C、X、Z、Q、Y、G |
| D、G、Q、Y、Z、X |
 如图所示,A池用石墨电极电解氢氧化钠溶液,B池精炼粗铜,一段时间后停止通电,A池D极产生的气体在标准状况下为2.24L.下列说法正确的是( )
如图所示,A池用石墨电极电解氢氧化钠溶液,B池精炼粗铜,一段时间后停止通电,A池D极产生的气体在标准状况下为2.24L.下列说法正确的是( )| A、A池为电解池,B池为原电池 |
| B、D电极与E电极都发生氧化反应 |
| C、F极是以粗铜板为材料 |
| D、B池中E极质量增加25.6g |
氧化还原反应的实质是( )
| A、得到氧元素与失去氧元素 |
| B、化合价的升降 |
| C、电子的得失或电子对的偏移 |
| D、有无新物质生成 |
2010年12月26日,中央电视台“焦点访谈”栏目播出《假蛋真相》,揭露部分制假者打着“人造鸡蛋技术”的幌子骗取培训费.据专家介绍,人造鸡蛋的蛋壳是用碳酸钙做的,蛋黄和蛋清则是用海藻酸钠、明矾、明胶、食用氯化钙加水、色素等制成.下列判断正确的是( )
| A、人造鸡蛋蛋清在硫酸铵.硫酸钠溶液中发生盐析;在硝酸铅溶液中变性 |
| B、用激光笔照射剥了壳的人造鸡蛋,会有光亮的“通路” |
| C、长期食用人造鸡蛋可以补钙,对人体健康有利 |
| D、人造鸡蛋长期放置会产生臭鸡蛋气味 |
下列反应中,属于吸热反应的是( )
| A、实验室制H2的反应 |
| B、实验室制CO2的反应 |
| C、氢氧化钡晶体与NH4Cl固体反应 |
| D、生石灰与水的反应 |