题目内容
2.下列气体易液化且遇挥发性酸时冒白烟,宜作制冷剂的是( )| A. | N2 | B. | NH3 | C. | NO | D. | NO2 |
分析 氨气易液化,液氨气化时吸热,因此液氨常用作制冷剂,氨气遇挥发性酸时冒白烟生成盐,氮气、一氧化氮、二氧化氮无该性质,据此分析解答.
解答 解:A.氮气沸点低,易液化,但气化时吸热少,不宜作制冷剂,遇挥发性酸时无白烟生成,故A错误;
B.氨气易液化,液氨气化时吸热,因此液氨常用作制冷剂,氨气遇挥发性酸时与酸反应生成铵盐冒白烟,如NH3+HCl=NH4Cl,故B正确;
C.一氧化氮沸点低,易液化,但气化时吸热少,不宜作制冷剂,遇挥发性酸时无白烟生成,故C错误;
D.二氧化氮为红棕色气体,沸点低,易液化,但气化时吸热少,不宜作制冷剂,遇挥发性酸时无白烟生成,故D错误;
故选B.
点评 本题考查氮的单质及其化合物的物理性质,题目难度不大,掌握氨气的物理性质是解答关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
12.生活中处处有化学,下列表述不正确的是( )
| A. | 福尔马林可作食品的保鲜剂 | |
| B. | 聚乙烯塑料制品可用于食品的包装 | |
| C. | 碳酸氢钠可作胃酸的中和剂 | |
| D. | 食盐可作调味剂,也可作食品防腐剂 |
13.分子式为C5H11Br且含有两个甲基的同分异构体共有(不考虑立体结构)( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
10.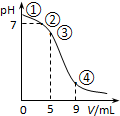 25℃时,向10mL 0.1mol•L-1 CH3COONa溶液中加入0.1mol•L-1盐酸,溶液pH随加入盐酸的体积变化情况如图所示.下列说法正确的是( )
25℃时,向10mL 0.1mol•L-1 CH3COONa溶液中加入0.1mol•L-1盐酸,溶液pH随加入盐酸的体积变化情况如图所示.下列说法正确的是( )
 25℃时,向10mL 0.1mol•L-1 CH3COONa溶液中加入0.1mol•L-1盐酸,溶液pH随加入盐酸的体积变化情况如图所示.下列说法正确的是( )
25℃时,向10mL 0.1mol•L-1 CH3COONa溶液中加入0.1mol•L-1盐酸,溶液pH随加入盐酸的体积变化情况如图所示.下列说法正确的是( )| A. | 点①所示溶液中:c(OH-)=c(H+)+c(CH3COOH) | |
| B. | 点②所示溶液中:c(CH3COOH)+c(CH3COO-)=0.05 mol•L-1 | |
| C. | 点③所示溶液中:c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-) | |
| D. | 点④所示溶液中:c(Na+)+c(H+)<c(CH3COO-)+c(Cl-) |
7.下列反应所得溶液中只含有一种溶质的是( )
| A. | 稀硝酸中加入过量铜片 | B. | Ca(OH)2溶液中通入Cl2 | ||
| C. | FeCl3溶液中加入过量铜片 | D. | AlCl3溶液中通入过量NaOH溶液 |
14.某溶液中大量存在Ba2+、H+、Cl-,该溶液中还可能大量存在的离子是( )
| A. | Ag+ | B. | SO42- | C. | CH3COO- | D. | Mg2+ |
11.下列各组化合物中,各化合物都有相同数目的同分异构体的是( )
| A. | CH2O与C2H4O2 | B. | C4H10与C4H6O | C. | CF2Cl2与C2F2Cl2 | D. | C4H10与C3H6 |
2.邻苯二甲酸酯类是最常见的塑化剂,实验室制备邻苯二甲酸二丁酯的反应原理如下,其中n-C4H9OH表示正丁醇.

已知:(1)上述反应的第一步进行得迅速而完全,第二步反应可逆,较难进行.
(2)有关物质的性质如下表所示:
实验步骤:装置图如1图所示,夹持装置、加热装置均略去.
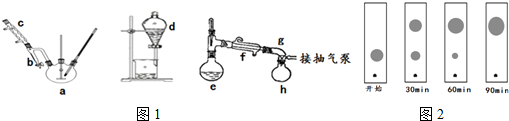
(Ⅰ)制备粗产品:在三颈烧瓶侧口插入温度计,另一侧口连接分水器与冷凝管,从中间口先加入3g(0.02mol)邻苯二甲酸酐及几粒沸石,在振摇下缓慢加入6.5mL(0.07mol)正丁醇和0.1mL浓硫酸的混合液.安装搅拌装置.在分水器中加入正丁醇至支管平齐.缓慢升温,使混合物微沸,至瓶内固体完全消失.继续回流,分水器中有小液滴沉入底部,当温度升到140℃时便可停止加热.
(Ⅱ)粗产品纯化:当反应液冷却到70℃以下时,将混合液转入分液漏斗,加入10mL 5% Na2CO3溶液洗涤,有机层用15mL温热的饱和食盐水洗涤2~3次,至有机层呈中性,分离出的油状物,用无水硫酸镁干燥,除去干燥剂.有机层先蒸去过量的正丁醇,最后在抽气泵的减压下蒸馏,收集180~190℃的馏分即得产品,称量质量.回答下列问题:
(1)仪器e的名称蒸馏烧瓶,浓硫酸的作用是催化剂,吸水剂抽气泵的作用是可降低有机物的沸点,可以防止有机物脱水碳化,提高产物的纯度.
(2)制备装置中冷凝水的流向与冷凝管中蒸汽的流向相同,制备过程中反应进行到终点的标志是分水器中的水位不再发生变化.
(3)产品纯化过程中,加入Na2CO3溶液的目的是将硫酸和 转变成盐,从而与产物分离,该操作是否可改用NaOH溶液?否(填“是”或“否”),原因是;氢氧化钠碱性太强,能使邻苯二甲酸二丁酯发生水解;.加入食盐水洗涤一方面是防止有机物发生乳化而不利于分层,另一方面是为了降低邻苯二甲酸二丁酯的溶解度.
转变成盐,从而与产物分离,该操作是否可改用NaOH溶液?否(填“是”或“否”),原因是;氢氧化钠碱性太强,能使邻苯二甲酸二丁酯发生水解;.加入食盐水洗涤一方面是防止有机物发生乳化而不利于分层,另一方面是为了降低邻苯二甲酸二丁酯的溶解度.
(4)实验中还可采用薄层色谱法(原理和操作与纸层析类同)跟踪反应进程,分别在反应开始后的不同时间,用毛细管从三颈烧瓶中取样、点样、薄层色谱展开后在紫外灯照射下(含苯环结构的物质可显色)斑点如图2.你认为不可能出现的情况是D.
A.开始 B.30min C.60min D.90min.

已知:(1)上述反应的第一步进行得迅速而完全,第二步反应可逆,较难进行.
(2)有关物质的性质如下表所示:
| 物质 | 性质(沸点及分解温度均为101kPa测得) |
| 邻苯二甲酸酐 (M=148g/mol) | 白色针状晶体.不溶于冷水,溶于热水及有机溶剂. 密度1.53g/cm3,沸点295℃. |
| 正丁醇(M=74g/mol) | 无色液体.微溶于水,溶于有机溶剂.密度0.81g/cm3,沸点117.7℃.可与水形成二元共沸物(沸点92.7℃). |
| 邻苯二甲酸二丁酯 (M=278g/mol) | 无色油状液体.难溶于水,溶于有机溶剂.密度1.49g/cm3,沸点340℃.酸性条件下180℃以上易发生分解. |

(Ⅰ)制备粗产品:在三颈烧瓶侧口插入温度计,另一侧口连接分水器与冷凝管,从中间口先加入3g(0.02mol)邻苯二甲酸酐及几粒沸石,在振摇下缓慢加入6.5mL(0.07mol)正丁醇和0.1mL浓硫酸的混合液.安装搅拌装置.在分水器中加入正丁醇至支管平齐.缓慢升温,使混合物微沸,至瓶内固体完全消失.继续回流,分水器中有小液滴沉入底部,当温度升到140℃时便可停止加热.
(Ⅱ)粗产品纯化:当反应液冷却到70℃以下时,将混合液转入分液漏斗,加入10mL 5% Na2CO3溶液洗涤,有机层用15mL温热的饱和食盐水洗涤2~3次,至有机层呈中性,分离出的油状物,用无水硫酸镁干燥,除去干燥剂.有机层先蒸去过量的正丁醇,最后在抽气泵的减压下蒸馏,收集180~190℃的馏分即得产品,称量质量.回答下列问题:
(1)仪器e的名称蒸馏烧瓶,浓硫酸的作用是催化剂,吸水剂抽气泵的作用是可降低有机物的沸点,可以防止有机物脱水碳化,提高产物的纯度.
(2)制备装置中冷凝水的流向与冷凝管中蒸汽的流向相同,制备过程中反应进行到终点的标志是分水器中的水位不再发生变化.
(3)产品纯化过程中,加入Na2CO3溶液的目的是将硫酸和
 转变成盐,从而与产物分离,该操作是否可改用NaOH溶液?否(填“是”或“否”),原因是;氢氧化钠碱性太强,能使邻苯二甲酸二丁酯发生水解;.加入食盐水洗涤一方面是防止有机物发生乳化而不利于分层,另一方面是为了降低邻苯二甲酸二丁酯的溶解度.
转变成盐,从而与产物分离,该操作是否可改用NaOH溶液?否(填“是”或“否”),原因是;氢氧化钠碱性太强,能使邻苯二甲酸二丁酯发生水解;.加入食盐水洗涤一方面是防止有机物发生乳化而不利于分层,另一方面是为了降低邻苯二甲酸二丁酯的溶解度.(4)实验中还可采用薄层色谱法(原理和操作与纸层析类同)跟踪反应进程,分别在反应开始后的不同时间,用毛细管从三颈烧瓶中取样、点样、薄层色谱展开后在紫外灯照射下(含苯环结构的物质可显色)斑点如图2.你认为不可能出现的情况是D.
A.开始 B.30min C.60min D.90min.
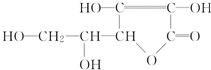 维生素C的结构简式如图所示:
维生素C的结构简式如图所示: