题目内容
已知95℃时水的离子积Kw=1×10-12,25℃时Kw=1×10-14,回答下列问题:
(1)95℃时水的电离常数________(填“>”“=”或“<”) 25℃时水的电离常数.
(2)95℃纯水中c(H+)________(填“>”、“=”或“<”)c(OH-).
(3)95℃时向纯水中加入NaOH,c(OH-)=1×10-1 mol/L,此时pH=________
> = 11
试题分析:(1)95℃时水的离子积Kw>25℃时Kw=1×10-14,95℃时电离程度大,所以95℃时水的电离常数大于25℃时水的电离常数。(2)95℃纯水中c(H+)=c(OH-).水是中性的,中性溶液中c(H+)=c(OH-)。(3)Kw=C(H+)·C(OH-)=1×10-12, c(OH-)=1×10-1 mol/L可知C(H+)=1×10-11 mol/L,PH=-lgC(H+)=11
考点:水离子积
点评:KW只与温度有关,本题是常考题,通过水离子积来计算酸碱性。
试题分析:(1)95℃时水的离子积Kw>25℃时Kw=1×10-14,95℃时电离程度大,所以95℃时水的电离常数大于25℃时水的电离常数。(2)95℃纯水中c(H+)=c(OH-).水是中性的,中性溶液中c(H+)=c(OH-)。(3)Kw=C(H+)·C(OH-)=1×10-12, c(OH-)=1×10-1 mol/L可知C(H+)=1×10-11 mol/L,PH=-lgC(H+)=11
考点:水离子积
点评:KW只与温度有关,本题是常考题,通过水离子积来计算酸碱性。

练习册系列答案
相关题目
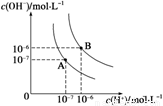
(1)水的电离平衡曲线如图所示,若A点表示25 ℃时水的电离达平衡时的离子浓度,B点表示95 ℃时水的电离达平衡时的离子浓度。则95℃时0.1 mol·L-1的NaOH溶液中,由水电离出的 c(H+)= mol·L-1,Kw(25 ℃) Kw(95℃)(填“>”、“<”或“=”)。25 ℃时,向水的电离平衡体系中加入少量NH4Cl 固体,对水的电离平衡的影响是 (填“促进”、“抑制”或“不影响”)。
(2)25℃时,在0.1L 0.2 mol·L-1的HA溶液中,有0.001mol的HA电离成离子,则该溶液的pH= ,电离度为 。
(3)电离平衡常数是衡量弱电解质电离程度强弱的量(已知如表数据)。向NaCN溶液中通入少量CO2,所发生反应的化学方程式为 。
|
化学式 |
电离平衡常数(25 ℃) |
|
HCN |
K=4.9×10-10 |
|
H2CO3 |
K1=4.3×10-7、K2=5.6×10-11 |
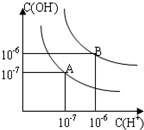 已知水在25℃和95℃时,其电离平衡曲线如图所示:
已知水在25℃和95℃时,其电离平衡曲线如图所示: