题目内容
重水 是重要的核工业原料,下列关于D原子的说法错误的是
是重要的核工业原料,下列关于D原子的说法错误的是
 是重要的核工业原料,下列关于D原子的说法错误的是
是重要的核工业原料,下列关于D原子的说法错误的是A.氘 原子核外有1个电子 原子核外有1个电子 | B.是H的同位素 |
| C.自然界中没有D原子存在 | D. 质量数为2 质量数为2 |
C
试题分析:A.氘
 原子核外有1个电子,正确。B.和H是由同种元素构成的不同原子,故为同位素关系,正确。C.自然界中存在D原子,错误。D.
原子核外有1个电子,正确。B.和H是由同种元素构成的不同原子,故为同位素关系,正确。C.自然界中存在D原子,错误。D. 质量数为2,正确。
质量数为2,正确。
练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案
相关题目
 2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如图所示。
2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如图所示。

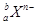 ,下列说法正确的是
,下列说法正确的是 g
g