题目内容
在温度和容积不变的条件下,有反应:2A(g)+2B(g)ƒC(g)+3D(g),现分别从两条途径建立平衡,(Ⅰ):A、B的起始浓度均为2 mol×L-1;(Ⅱ):C、D的起始浓度分别为2 mol×L-1,6 mol×L-1下列叙述正确的是( )
A.两途径最终达平衡时,(Ⅰ)体系内各气体的物质的量的分数与(Ⅱ)体系的相同
B.两途径最终达平衡时,(Ⅰ)体系内各气体的体积分数与(Ⅱ)体系的不同
C.达平衡时,(Ⅰ)中的反应速率,v(A)等于(Ⅱ)中的v(A)
D.达平衡时,(Ⅰ)的混合气体密度与(Ⅱ)的相等
答案:A
解析:
解析:
(Ⅱ)的C、D折算成A、B分别4mol×L-1,即为(Ⅰ)的两倍,而此反应为反应前后气体的物质的量相等的反应,所以(Ⅰ)(Ⅱ)建立的是等效平衡,只是各物质的量(Ⅱ)为(Ⅰ)中对应的两倍,所以各气体的物质的量的分数相同,体积分数也相同,因(Ⅰ)(Ⅱ)中体积相等,所以各物质的浓度(Ⅱ)中为(Ⅰ)的两倍,所以密度不同,反应速率也不同。
|

练习册系列答案
相关题目
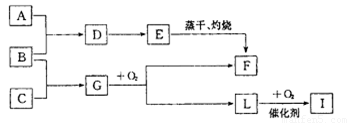
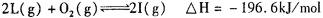 。向一个容积不变的 容器中,充入2mol L和1molO2,使之充分反应,放出的热量为Q,则Q_______196. 6kJ (填“ >”、“〈”或“=”)。
。向一个容积不变的 容器中,充入2mol L和1molO2,使之充分反应,放出的热量为Q,则Q_______196. 6kJ (填“ >”、“〈”或“=”)。