题目内容
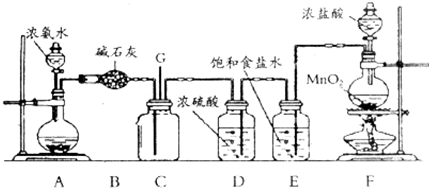
19.实验室制乙烯时,常因温度过高和浓H2SO4的强氧化性而发生副反应:CH3CH2OH+4H2SO4 $\stackrel{△}{→}$ 4SO2↑+CO2↑+7H2O+C,所制乙烯也因此混有SO2、CO2和水蒸气,如图装置,回答问题:
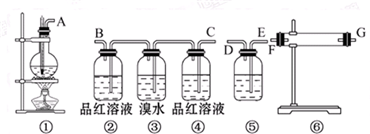
(1)用上述实验装置设计一个实验,以验证制得的乙烯中含有SO2、CO2和水蒸气,这些实验装置的连接顺序是A→F→G→C→B→E→D(F、G可换)(用A、B、C、D…表示).
(2)实验时②中现象品红退色,结论是乙烯气体中含有SO2;洗气瓶③中现象是溴水退色,作用是将SO2完全吸收或除去SO2;
(3)装置⑥中加的固体药品是无水CuSO4,以验证乙烯中含有水蒸气;
(4)装置⑤中盛有的溶液是澄清石灰水,以验证乙烯中含有CO2.
分析 (1)验证制得的乙烯中含有SO2、CO2和水蒸气,需要先检验水,再检验并除去二氧化硫,最后检验二氧化碳,据此连接装置;
(2)根据二氧化硫检验漂白性分析实验时②中的现象及结论;二氧化硫检验还原性,能够被二氧化硫氧化,则用集气瓶③中的溴水除去二氧化硫;
(3)装置⑥用于检验水,检验乙烯中含有的水蒸气选用无水硫酸铜;
(4)装置⑤用于检验二氧化碳气体,通常使用澄清石灰水.
解答 解:(1)制乙烯时含有SO2、CO2和水蒸气,检验杂质气体时一定要注意先后顺序:检验水蒸气的存在一定要用无水CuSO4,该操作应先进行,否则即使是干燥的气体经过溶液也会带有水蒸气,影响对水蒸气的检验;检验CO2要用到澄清石灰水,而SO2也会使石灰水变浑浊,因此应先检验SO2气体,并除去SO2气体后,再检验CO2,SO2可使品红退色可以用来检验SO2气体;在③中除去SO2气体 (SO2+Br2+2H2O═H2SO4+2HBr),若②中品红不退色,说明SO2被除尽,通过⑤检验CO2气体,所以②③④应放在装置⑥之后⑤之前,所以装置连接顺序为:A→F→G→C→B→E→D(F、G可换),
故答案为:A→F→G→C→B→E→D(F、G可换);
(2)二氧化硫检验漂白性,能够使品红溶液褪色,则实验时②中品红溶液褪色,证明混合气体中含有二氧化硫气体;二氧化硫能够被溴水氧化,所以集气瓶③中溴水退色,目的是将混合气体中的SO2完全吸收或除去SO2,
故答案为:品红退色;乙烯气体中含有SO2;溴水退色;将SO2完全吸收或除去SO2;
(3)装置⑥中中盛放的是无水硫酸铜,用于检验乙烯中是否混有水蒸气,
故答案为:无水CuSO4;水蒸气;
(4)装置⑤盛放的是澄清石灰水,用于检验乙烯中是否含有二氧化碳气体,
故答案为:澄清石灰水;CO2.
点评 本题主要考查实验室制乙烯的反应产物的检验方法,题目难度中等,当有多种产物需检验时,应考虑先后顺序,在除去杂质气体时不能引入新杂质.

(1)第一份加入几滴AgNO3溶液后有沉淀产生;
(2)第二份加过量NaOH溶液加热后,只收集到气体0.03mol,无沉淀生成,同时得到溶液甲
(3)在甲溶液中通入过量CO2,生成白色沉淀,沉淀经过滤、洗涤、灼烧,质量为1.02g
(4)第三份加足量BaCl2溶液后,得白色沉淀,沉淀经足量盐酸洗涤、干燥后,质量为11.65g.
下列说法不正确的是( )
| A. | 步骤(3)后可以确定CO32-一定不存在 | |
| B. | 忽略步骤(1)对实验结论并无影响 | |
| C. | 不能确定原溶液是否含有K+和Cl- | |
| D. | 若把步骤(2)产生的气体通入步骤(1)的滤液中,又可产生0.78g沉淀 |
①铷是有较高熔点的金属单质
②铯在化合物中呈+1价
③锂可能与水反应,但不熔化成小球
④锂金属性很活泼,故要保存在煤油中
⑤钾单质与水反应剧烈,会在水中上下浮动.
| A. | ②③④ | B. | ①③⑤ | C. | ①②⑤ | D. | ①④⑤ |
| A. | NH3 | B. | SO2 | C. | CH4 | D. | H2 |

 ;
; 、
、 ;
; .
. ;
; 有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取.纯净的A为无色黏稠液体,易溶于水.为研究A的组成与结构,进行了如下实验:
有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取.纯净的A为无色黏稠液体,易溶于水.为研究A的组成与结构,进行了如下实验: .
.