题目内容
8.①司机是否酒后驾车,可通过对其呼出的气体进行检验而查出,所利用的化学反应为2CrO3(红色)+3C2H5OH+3H2SO4═Cr2(SO4)3(绿色)+3CH3CHO+6H2O被检测的气体的成分是C2H5OH,上述反应中的氧化剂是CrO3.还原剂是C2H5OH.
②1866年凯库勒提出了苯的单、双键交替的正六边形平面结构,解释了苯的部分性质,但还有一些问题尚未解决,它不能解释下列ad事实(填入编号).
a.苯不能使溴的四氯化碳溶液褪色 b.苯能与H2发生加成反应 c.苯没有同分异构体 d.邻二溴苯只有一种现代化学认为苯分子碳碳之间的键是介于单键和双键之间的特殊的键.
分析 ①化合价升高被氧化的为还原剂,化合价降低被还原的为氧化剂,根据反应物及化合价的变化判断;
②根据双键能发生加成反应分析性质,根据Br-C-C-Br和Br-C=C-Br两种不同的位置分析结构;苯分子中含有一种特殊的化学键,键长介于C-C和C=C之间,不存在单纯的单、双键.
解答 解:①由题意知,被检测的物质是乙醇,反应2CrO3 (红色)+3C2H5OH+3H2SO4=Cr2(SO4)3(绿色)+3CH3CHO+6H2O中,元素的化合价变化如下:CrO3→Cr2(SO4)3,Cr元素由+6价→+3价,得电子化合价降低,CrO3是氧化剂;C2H5OH→CH3CHO,C元素由-2价→-1价,失电子化合价升高,乙醇是还原剂,
故答案为:C2H5OH;CrO3;C2H5OH;
②a.若苯分子中含有C=C键,则能发生加成反应而使溴的四氯化碳溶液褪色,但苯不能使溴的四氯化碳溶液褪色,故a选;
b.苯能与H2发生加成反应,能够用苯分子中含有碳碳双键解释,故b不选;
c.苯为单、双键交替的正六边形平面结构,可以解释苯没有同分异构体,故c不选;
d.如果是单双建交替的正六边形平面结构,则邻二溴苯应有Br-C-C-Br和Br-C=C-Br两种不同的结构,但事实是邻二溴苯只有一种,这一点也不能解释,故d选;
苯分子中含有一种特殊的化学键,键长介于C-C和C=C之间,不存在单纯的单、双键,是介于碳碳单键和碳碳双键之间的特殊的键,
故答案为:ad;介于单键和双键之间的特殊的键.
点评 本题考查氧化还原反应、苯的组成及结构,题目难度不大,明确氧化还原反应的实质为解答关键,注意掌握常见有机物组成、结构与性质,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
16.下列有关硅及其化合物的说法中正确的是( )
| A. | 硅酸钠属于盐,不属于碱,所以硅酸钠可以保存在磨口玻璃塞试剂瓶中 | |
| B. | 氢氟酸可用带橡胶塞的玻璃试剂瓶保存 | |
| C. | 普通玻璃、石英玻璃、水泥等均属于硅酸盐材料 | |
| D. | 祖母绿的主要成分为Be3Al2Si6O18,用氧化物形式表示为3BeO•Al2O3•6SiO2 |
19.下列关于有机物的说法不正确的是( )
| A. | 相同条件下的沸点:丙三醇>乙二醇>乙醇>乙烷>甲烷 | |
| B. | 将浸透了石蜡油的石棉放在大试管底部,大试管中加入碎瓷片,加强热,将产生的气体持续通入溴的四氯化碳溶液中,红棕色逐渐变浅,最终褪色 | |
| C. | -C3H7和-C2H5O各取代苯分子中的一个氢原子形成的二元取代物的同分异构体有24种 | |
| D. | 薄荷醇 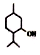 中至少有12个原子共平面 中至少有12个原子共平面 |
16.下列说法正确的是( )
| A. | 丙烷的比例模型是 | B. | C2H4 与C3H6不一定互为同系物 | ||
| C. |  属于苯的同系物 属于苯的同系物 | D. |  和 和 互为同分异构体 互为同分异构体 |
13.短周期主族元素W、R、X、Y、Z的原子序数依次增大,且分占三个不同的周期.W与X同主族,R与Z同主族,R原子最外层电子数是其内层电子数的3倍,Y是地壳中含量最多的金属元素.下列说法中正确的是( )
| A. | W、X是金属元素 | |
| B. | 原子半径:R<Y<Z | |
| C. | 简单气态氢化物的热稳定性:R>Z | |
| D. | X、Y、Z的最高价氧化物对应的水化物能相互反应 |
20.某一化学反应,在1L的密闭容器中,气态反应物B的物质的量在5s内从2.0mol变成0.5mol,在这5s内B的化学反应速率为( )
| A. | 3mol/(L•s) | B. | 0.3mol/(L•s) | C. | 0.6mol/(L•s) | D. | 0.1mol/(L•s) |
17.下列叙述正确的是( )
| A. | 在氧化还原反应中,一定是有一种元素被氧化,另一种元素被还原 | |
| B. | 没有单质参加或生成的反应一定不是氧化还原反应 | |
| C. | 失电子难的原子,获得电子的能力一定强 | |
| D. | 元素由化合态变成游离态时,它可能被氧化,也可能被还原 |
2.催化还原CO2是解决温室效应及能源问题的重要手段之一.研究表明,在Cu/ZnO催化剂存在下,CO2和H2可发生两个平行反应,分别生成CH3OH和CO.反应的热化学方程式如下:
Ⅰ. CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H1=-53.7kJ•mol-1 K1
Ⅱ. CO2(g)+H2(g)?CO(g)+H2O(g)△H2 K2
(1)反应Ⅰ的平衡常数表达式K1=$\frac{c(C{H}_{3}OH)•c({H}_{2}O)}{c(C{O}_{2})•{c}^{3}({H}_{2})}$.若其它条件不变,升高温度,则该反应的逆反应速率增大(填“增大”、“减小”、“不变”或“无法判断”).
(2)反应Ⅱ还可以通过下列反应获得:
Fe(s)+CO2(g)?FeO(s)+CO(g)△H3 K3
Fe(s)+H2O(g)?FeO(s)+H2(g)△H4 K4
在不同温度时K3、K4的值如下表1:
请回答(不考虑温度对△H的影响):
△H2=△H3-△H4(用△H3和△H4表示),K2=$\frac{{K}_{3}}{{K}_{4}}$ (用K3和K4表示),反应Ⅱ属于吸热反应(填“放热”或“吸热”).
(3)某实验室控制CO2和H2初始投料比为1:2.2,在相同压强下,经过相同反应时间测得如下表2实验数据:
【备注】Cat.1:$\frac{Cu}{ZnO}$纳米棒;Cat.2:Cu/ZnO纳米片;甲醇选择性:转化的CO2中生成甲醇的百分比.
①在Cu/ZnO催化剂存在下,有利于提高CO2转化为CH3OH平衡转化率的措施有CD.
A.使用催化剂Cat.1 B.使用催化剂Cat.2 C.降低反应温度
D.投料比不变,增加反应物的浓度 E.增大CO2和H2的初始投料比
②表2中实验数据表明,在相同温度下不同的催化剂对CO2转化成CH3OH的选择性有显著的影响,其原因是表中数据表明此时未达到平衡,不同的催化剂对反应Ⅰ的催化能力不同,因而在该时刻下对甲醇选择性有影响.
Ⅰ. CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H1=-53.7kJ•mol-1 K1
Ⅱ. CO2(g)+H2(g)?CO(g)+H2O(g)△H2 K2
(1)反应Ⅰ的平衡常数表达式K1=$\frac{c(C{H}_{3}OH)•c({H}_{2}O)}{c(C{O}_{2})•{c}^{3}({H}_{2})}$.若其它条件不变,升高温度,则该反应的逆反应速率增大(填“增大”、“减小”、“不变”或“无法判断”).
(2)反应Ⅱ还可以通过下列反应获得:
Fe(s)+CO2(g)?FeO(s)+CO(g)△H3 K3
Fe(s)+H2O(g)?FeO(s)+H2(g)△H4 K4
在不同温度时K3、K4的值如下表1:
| 700℃ | 900℃ | |
| K3 | 1.47 | 2.15 |
| K4 | 2.38 | 1.67 |
△H2=△H3-△H4(用△H3和△H4表示),K2=$\frac{{K}_{3}}{{K}_{4}}$ (用K3和K4表示),反应Ⅱ属于吸热反应(填“放热”或“吸热”).
(3)某实验室控制CO2和H2初始投料比为1:2.2,在相同压强下,经过相同反应时间测得如下表2实验数据:
| T(K) | 催化剂 | CO2转化率(%) | 甲醇选择性(%) |
| 543 | Cat.1 | 12.3 | 42.3 |
| 543 | Cat.2 | 10.9 | 72.7 |
| 553 | Cat.1 | 15.3 | 39.1 |
| 553 | Cat.2 | 12.0 | 71.6 |
①在Cu/ZnO催化剂存在下,有利于提高CO2转化为CH3OH平衡转化率的措施有CD.
A.使用催化剂Cat.1 B.使用催化剂Cat.2 C.降低反应温度
D.投料比不变,增加反应物的浓度 E.增大CO2和H2的初始投料比
②表2中实验数据表明,在相同温度下不同的催化剂对CO2转化成CH3OH的选择性有显著的影响,其原因是表中数据表明此时未达到平衡,不同的催化剂对反应Ⅰ的催化能力不同,因而在该时刻下对甲醇选择性有影响.
