题目内容
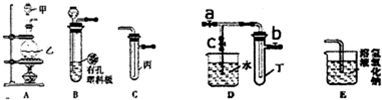
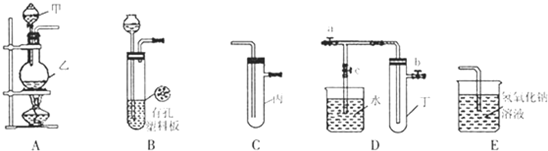
利用如图所示实验装置完成比较乙酸、碳酸和苯酚的羟基中氢原子的活泼性实验.
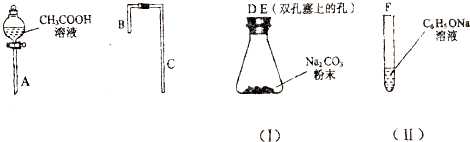
(1)利用如图所示仪器组装实验装置,其中A管接
(2)丙同学查资料发现乙酸有挥发性,于是在试管F之前增加了一个盛有
(3)完成装置中反应方程式(Ⅰ)

(1)利用如图所示仪器组装实验装置,其中A管接
D(或E)
D(或E)
(填字母,下同)口,B管接E(或D)
E(或D)
口,C管接F
F
中.(2)丙同学查资料发现乙酸有挥发性,于是在试管F之前增加了一个盛有
饱和NaHCO3
饱和NaHCO3
溶液的洗气装置,使乙同学的实验设计更加完善.(3)完成装置中反应方程式(Ⅰ)
2CH3COOH+Na2CO3=2CH3COONa+CO2↑+H2O
2CH3COOH+Na2CO3=2CH3COONa+CO2↑+H2O
;(Ⅱ)C6H5ONa+CO2+H2O=C6H5OH+NaHCO3
C6H5ONa+CO2+H2O=C6H5OH+NaHCO3
;(Ⅲ)中实验现象产生白色沉淀
产生白色沉淀
.分析:(1)根据实验目的,以及所发生的化学反应,确定实验方案的设;
(2)试管F之前增加了一个盛有饱和NaHCO3溶液的洗气装置,目的是将二氧化碳中的乙酸洗去,防止乙酸与苯酚钠反应;
(3)反应(Ⅰ)是醋酸与碳酸钠的反应,反应(Ⅱ)是二氧化碳与苯酚钠溶液的反应,(Ⅲ)中苯酚钠和二氧化碳、水反应生成碳酸氢钠、苯酚,由于苯酚的溶解性较小而析出.
(2)试管F之前增加了一个盛有饱和NaHCO3溶液的洗气装置,目的是将二氧化碳中的乙酸洗去,防止乙酸与苯酚钠反应;
(3)反应(Ⅰ)是醋酸与碳酸钠的反应,反应(Ⅱ)是二氧化碳与苯酚钠溶液的反应,(Ⅲ)中苯酚钠和二氧化碳、水反应生成碳酸氢钠、苯酚,由于苯酚的溶解性较小而析出.
解答:解:(1)比较乙酸、碳酸和苯酚的羟基中氢原子的活泼性,实验目的是证明酸性:乙酸>碳酸>苯酚,根据强酸制取弱酸的原则,须设计酸性:乙酸>碳酸>苯酚,即乙酸和碳酸钠反应生成二氧化碳,所以A连接D;将生成的二氧化碳通入苯酚钠溶液中,二氧化碳、水和苯酚钠反应生成苯酚和碳酸氢钠,所以C连接F,
故答案为:D(或E);E(或D);F;
(2)在试管F之前增加了一个盛有饱和NaHCO3溶液的洗气装置,目的是将二氧化碳中的乙酸洗去,防止乙酸与苯酚钠反应,
故答案为:饱和NaHCO3.
(3)反应(Ⅰ)为醋酸与碳酸钠的反应,反应方程式为:2CH3COOH+Na2CO3=2CH3COONa+CO2↑+H2O,
反应(Ⅱ)是二氧化碳与苯酚钠溶液的反应,反应方程式为:C6H5ONa+CO2+H2O=C6H5OH+NaHCO3,
(Ⅲ)中苯酚钠和二氧化碳、水反应生成碳酸氢钠、苯酚,由于苯酚的溶解性较小而析出,
故答案为:2CH3COOH+Na2CO3=2CH3COONa+CO2↑+H2O;C6H5ONa+CO2+H2O=C6H5OH+NaHCO3;产生白色沉淀.
故答案为:D(或E);E(或D);F;
(2)在试管F之前增加了一个盛有饱和NaHCO3溶液的洗气装置,目的是将二氧化碳中的乙酸洗去,防止乙酸与苯酚钠反应,
故答案为:饱和NaHCO3.
(3)反应(Ⅰ)为醋酸与碳酸钠的反应,反应方程式为:2CH3COOH+Na2CO3=2CH3COONa+CO2↑+H2O,
反应(Ⅱ)是二氧化碳与苯酚钠溶液的反应,反应方程式为:C6H5ONa+CO2+H2O=C6H5OH+NaHCO3,
(Ⅲ)中苯酚钠和二氧化碳、水反应生成碳酸氢钠、苯酚,由于苯酚的溶解性较小而析出,
故答案为:2CH3COOH+Na2CO3=2CH3COONa+CO2↑+H2O;C6H5ONa+CO2+H2O=C6H5OH+NaHCO3;产生白色沉淀.
点评:本题考查了比较弱酸相对强弱的方法,注意根据酸性乙酸>碳酸>苯酚设计实验,实验设计根据实验目的进行设计,本题难度不大.

练习册系列答案
相关题目