题目内容
常温下,在25mL 0.1mol?L-1NaOH溶液中逐滴加入amL 0.2mol?L-1 CH3COOH溶液,有关混合溶液的判断正确的是( )
| A.当pH=7时,一定有:c(Na+)=c(CH3COO-)=c(OH-)=c(H+) |
| B.当a=25时,一定有:c(CH3COO-)+c(CH3COOH)=c(Na+) |
| C.当c(CH3COO-)>c(Na+)时,a一定大于12.5 |
| D.当c(OH-)>c(H+)时,a一定小于12.5 |
A、当pH=7时,根据溶液电中性可知,c(Na+)+c(H+)=c(CH3COO-)+c(OH-),则c(Na+)=c(CH3COO-),c(OH-)=c(H+),此时c(Na+)=c(CH3COO-)>c(OH-)=c(H+),故A错误;
B、当a=25时,醋酸过量,是NaOH物质的量的2倍,应有c(CH3COO-)+c(CH3COOH)=2c(Na+),故B错误;
C、根据溶液电中性可知,c(Na+)+c(H+)=c(CH3COO-)+c(OH-),当c(CH3COO-)>c(Na+)时,c(OH-)<c(H+),溶液呈酸性,醋酸过量,a一定大于12.5,故C正确;
D、a=12.5时,恰好反应生成醋酸钠溶液,水解呈碱性,所以当c(OH-)>c(H+)时,a不一定小于12.5,故D错误.
故选C.
B、当a=25时,醋酸过量,是NaOH物质的量的2倍,应有c(CH3COO-)+c(CH3COOH)=2c(Na+),故B错误;
C、根据溶液电中性可知,c(Na+)+c(H+)=c(CH3COO-)+c(OH-),当c(CH3COO-)>c(Na+)时,c(OH-)<c(H+),溶液呈酸性,醋酸过量,a一定大于12.5,故C正确;
D、a=12.5时,恰好反应生成醋酸钠溶液,水解呈碱性,所以当c(OH-)>c(H+)时,a不一定小于12.5,故D错误.
故选C.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
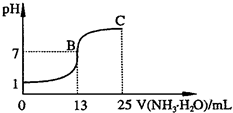 (2011?青岛模拟)氮的化合物在某些领域中扮演着重要的角色.
(2011?青岛模拟)氮的化合物在某些领域中扮演着重要的角色.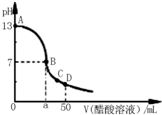 常温下,向25mL 0.1mol?L-1 NaOH溶液中逐滴加入0.1 mol?L-1 CH3COOH溶液,曲线如图所示,有关粒子浓度关系正确的是( )
常温下,向25mL 0.1mol?L-1 NaOH溶液中逐滴加入0.1 mol?L-1 CH3COOH溶液,曲线如图所示,有关粒子浓度关系正确的是( )