题目内容
有关①100ml 0.1 mol/L 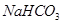 、②100ml 0.1 mol/L
、②100ml 0.1 mol/L  两种溶液的叙述不正确的是(
两种溶液的叙述不正确的是(
| A.①溶液中:c(CO32-)> c(H2CO3) | B.溶液中阴离子的物质的量浓度之和:②>① |
C.溶液中水电离出的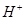 个数:②>① 个数:②>① | D.②溶液中: c(HCO3-)> c(H2CO3) |
A
解析试题分析:碳酸氢钠的水解程度大于碳酸氢钠的电离程度,所以碳酸氢钠溶液显碱性,因此碳酸氢钠溶液中c(CO32-)<c(H2CO3),A不正确;碳酸钠的水解程度大于碳酸氢钠的,所以碳酸钠溶液的碱性大于碳酸氢钠溶液的碱性,因此选项B、C、D都是正确的,答案选A。
考点:考查碳酸钠和碳酸氢钠溶液中离子浓度大小比较
点评:该题是高考中的常见考点,属于中等难度的试题。试题基础性强,注重考查学生分析问题、解决问题的能力,有利于培养学生严谨的逻辑思维能力以及灵活应变能力。该题的关键是灵活运用电荷守恒、物料守恒、质子守恒。

练习册系列答案
相关题目
有关①100ml 0.1mol/L NaHCO3、②100ml 0.1mol/L Na2CO3两种溶液的叙述不正确的是( )
| A、溶液中水电离出的H+个数:②>① | B、溶液中阴离子的物质的量浓度之和:②>① | C、①溶液中:c(CO32-)>c(H2CO3) | D、②溶液中:c(HCO3-)>c(H2CO3) |