题目内容
下列各组物质相互混合反应后,最终有白色沉淀生成的是( )
①金属钠投入到FeCl3溶液中
②过量Ba(OH)2溶液和明矾溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中
④向NaAlO2溶液中通入过量CO2
⑤向饱和Na2CO3溶液中通入足量CO2.
①金属钠投入到FeCl3溶液中
②过量Ba(OH)2溶液和明矾溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中
④向NaAlO2溶液中通入过量CO2
⑤向饱和Na2CO3溶液中通入足量CO2.
| A、只有②③④⑤ | B、只有①②⑤ |
| C、只有②③⑤ | D、全部 |
考点:钠的化学性质,钠的重要化合物,镁、铝的重要化合物
专题:元素及其化合物
分析:根据复分解反应发生的条件及物质的溶解性来分析能够反应且有沉淀生成,注意沉淀必须是白色的,据此分析解答.
①最终得到红褐色Fe(OH)3沉淀;②Ba(OH)2过量,最终只有白色硫酸钡沉淀;③最终由碳酸钙沉淀;④最终由氢氧化铝白色沉淀;⑤最终有碳酸氢钠白色沉淀.
①最终得到红褐色Fe(OH)3沉淀;②Ba(OH)2过量,最终只有白色硫酸钡沉淀;③最终由碳酸钙沉淀;④最终由氢氧化铝白色沉淀;⑤最终有碳酸氢钠白色沉淀.
解答:
解:①金属钠投入到烧杯中的FeCl2溶液中,发生的反应为:2Na+2H2O=2NaOH+H2 ↑,3NaOH+FeCl3=Fe(OH)3↓+3NaCl,所以最终生成的沉淀是红褐色的,所以不符合,故①错误;
②过量Ba(OH)2溶液和明矾溶液混合Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O,最终只有白色硫酸钡沉淀,故②正确;
③少量Ca(OH)2投入过量NaHCO3溶液中发生的反应为:Ca(OH)2+2NaHCO3=CaCO3 ↓+2H2O+Na2CO3,碳酸钙是白色沉淀,所以有白色沉淀生成,故③正确;
④向NaAlO2溶液中通入过量的CO2,二氧化碳过量,偏铝酸钠溶液与二氧化碳反应生成了氢氧化铝和碳酸氢钠,沉淀不溶解,所以符合条件,故④正确;
⑤向饱和Na2CO3溶液中通入足量CO2发生的反应为:Na2CO3+H2O+CO2=2NaHCO3,碳酸氢钠的溶解性小于碳酸钠的溶解性,所以向饱和Na2CO3溶液中通入足量CO2会析出碳酸氢钠晶体,所以产生白色沉淀,故⑤正确;
故选A.
②过量Ba(OH)2溶液和明矾溶液混合Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O,最终只有白色硫酸钡沉淀,故②正确;
③少量Ca(OH)2投入过量NaHCO3溶液中发生的反应为:Ca(OH)2+2NaHCO3=CaCO3 ↓+2H2O+Na2CO3,碳酸钙是白色沉淀,所以有白色沉淀生成,故③正确;
④向NaAlO2溶液中通入过量的CO2,二氧化碳过量,偏铝酸钠溶液与二氧化碳反应生成了氢氧化铝和碳酸氢钠,沉淀不溶解,所以符合条件,故④正确;
⑤向饱和Na2CO3溶液中通入足量CO2发生的反应为:Na2CO3+H2O+CO2=2NaHCO3,碳酸氢钠的溶解性小于碳酸钠的溶解性,所以向饱和Na2CO3溶液中通入足量CO2会析出碳酸氢钠晶体,所以产生白色沉淀,故⑤正确;
故选A.
点评:本题考查了物质性质的分析应用,主要是试剂量不同产物本题的产物判断,反应现象的分析应用,掌握物质性质是解题关键,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列反应的产物中,有的有同分异构体,有的没有同分异构体,其中一定不存在同分异构体的反应是( )
| A、1,3-丁二烯(CH2=CH-CH=CH2)与等物质的量的Br2发生加成反应 |
B、2-氯丁烷 与NaOH乙醇溶液共热发生消去HCl分子的反应 与NaOH乙醇溶液共热发生消去HCl分子的反应 |
| C、丙炔与足量的溴水发生的加成反应 |
| D、CH2=CH-CH3与HBr发生的加成反应 |
向盛有硝酸银水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到无色的透明溶液,下列对此现象的说法正确的是( )
| A、反应前后Ag+的浓度不变 |
| B、沉淀溶解后,生成[Ag(NH3)2]OH难电离 |
| C、配合离子[Ag(NH3)2]+ 存在离子键和共价键 |
| D、配合离子[Ag(NH3)2]+中,Ag+提供空轨道,NH3给出孤对电子 |
下列实验对应的结论正确的是( )
A、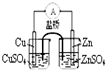 如图能组成Zn、Cu原电池 |
B、 如图能证明非金属性C>Si |
C、 如图说明反应2NO2?N2O4,△H>0 |
D、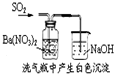 如图白色沉淀为BaSO3 |
关于化学反应中的能量变化,下列说法中不正确的是( )
| A、燃烧反应都是放热反应 |
| B、对于可逆反应:aA(g)+bB(g)?bC(g)+dD(g),如果正反应放热,逆反应一定吸热 |
| C、氢气燃烧生成水是一个放热的化学反应,说明1mol H2的能量高于1mol H2O的能量 |
| D、只有放热的氧化还原反应才可以设计为原电池 |
美国科学家罗伯特?莱夫科维茨和布莱恩?克比尔卡因“G 蛋白偶联受体研究”而获得2012年诺贝尔化学奖,他们将碘的同位素附着到各种激素上,借助放射学找到一些受体,进一步研究出“G 蛋白偶联受体”发挥的作用和机理,下列有关说法正确的是( )
A、放射性同位素
| ||
| B、蛋白质是生物体维持生命活动所需能量的主要来源 | ||
| C、动物蛋白质和植物蛋白质混合摄入,更能增强蛋白质的营养作用 | ||
| D、“春蚕到死丝方尽,蜡烛成灰泪始干”其中的“丝”和“泪”化学成分都是蛋白质 |
能显著地促进藻类在水中生长,最终导致水中生物缺氧的阴离子是( )
| A、Cl- |
| B、I- |
| C、CO32- |
| D、PO43- |
实验室通常悬挂涂有CuI的滤纸监测空气中汞蒸气的含量.反应方程式为:4CuI+Hg═Cu2HgI4+2Cu,下列叙述正确的是( )
| A、4mol CuI反应后得到2mol电子 |
| B、4mol CuI反应后失去4mol电子 |
| C、lmol Hg反应后得到2mol电子 |
| D、1mol Hg反应后失去4mol电子 |