题目内容
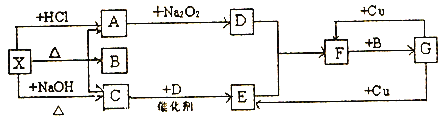
【题目】(1)把对应物质的字母代码填入括号内.
A.水玻璃 B.明矾 C.浓硫酸 D.过氧化钠 E.新制氯水 F.小苏打 G次氯酸钙
①能使石蕊试液先变红后褪色___________。
②能做木材防火剂___________。
③能做处理胃酸过多的一种药剂____________。
(2)综合考虑经济、技术、环保等方面因素,设计以铜为原料制取硫酸铜的最佳路线图。如:![]()
路线图为:________________。
【答案】E A F ![]()
【解析】
(1).①.使石蕊试液先变红后褪色的物质具有酸性和强氧化性,因新制氯水中含有盐酸和次氯酸,则应为新制氯水,故答案为:E;
②. 硅酸钠是耐火材料,能做木材防火剂,故答案为:A;
③. 能做处理胃酸过多的一种药剂,必须是可以和盐酸反应且不具有毒性和腐蚀性的物质,可以选择碳酸氢钠,故答案为:F;
(2). 以铜为原料制取硫酸铜,综合考虑经济、技术、环保等方面因素,应先生成氧化铜,氧化铜与硫酸反应生成硫酸铜,反应的方程式为2Cu+O2![]() 2CuO、CuO+H2SO4=CuSO4+H2O,路线图为:
2CuO、CuO+H2SO4=CuSO4+H2O,路线图为:![]() ,故答案为:
,故答案为:![]() 。
。

练习册系列答案
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案
相关题目