题目内容
8.以下非金属氧化物与其引起的环境问题及主要来源对应正确的是( )| 选项 | 氧化物 | 环境问题 | 主要来源 |
| A | CO2 | 破坏臭氧层 | 化石燃料的燃烧 |
| B | SO2 | 温室效应 | 汽车尾气的排放 |
| C | NO2 | 光化学烟雾 | 工厂废气的排放 |
| D | CO | 酸雨 | 汽车尾气和化石燃料的不完全燃烧 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.二氧化碳与温室效应有关;
B.二氧化硫与酸雨有关,温室效应的罪魁祸首是二氧化碳;
C.二氧化氮与光化学烟雾有关;
D.燃料不完全燃烧生成CO,CO有毒,CO与酸雨无关.
解答 解:A.化石燃料燃烧主要排放二氧化碳气体,与温室效应有关,而与破坏臭氧层无关,故A错误;
B.工厂废气的排放产生大量二氧化硫气体,是形成酸雨的主要污染物,而温室效应是由二氧化碳引起的,故B错误;
C.汽车尾气排放大量的氮氧化物,氮氧化物是形成光化学烟雾的主要污染物,故C正确;
D.形成酸雨与二氧化硫及氮的氧化物有关,CO是一种有毒气体,与酸雨无关,故D错误;
故选C.
点评 本题考查常见的生活环境的污染治理,题目难度不大,注意掌握污染物的形成条件及防治方法,试题侧重基础知识的考查,培养了学生的环境保护意识.

练习册系列答案
相关题目
19.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 0.1mol${\;}_{\;}^{16}$OD-离子含有的电子、中子数均为1.0NA | |
| B. | 标准状况下,4.48L己烷含有的分子数为0.2NA | |
| C. | 总质量为5.6g的CaO和CaC2混合物中,所含离子总数小于0.2NA | |
| D. | 常温常压下,0.1molNH3与0.1molHCl充分反应后所得产物含0.1NA个分子 |
16.除去CO2中混有的少量SO2气体,不可选用的试剂是( )
| A. | KMnO4溶液 | B. | NaClO溶液 | C. | 饱和NaHCO3溶液 | D. | 饱和Na2CO3溶液 |
3.洋蓟属高档蔬菜,从洋蓟提取的物质A具有良好的保健功能和药用价值,A在酸性条件下水解可生成B和C,反应可表示为
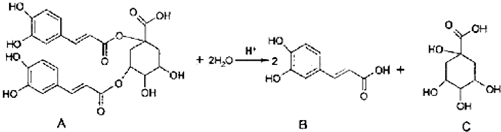
下列说法不正确的是 ( )

下列说法不正确的是 ( )
| A. | 1mol A和足量NaOH溶液反应,最多消耗11molNaOH | |
| B. | A在一定条件下能发生取代反应、加成反应和消去反应 | |
| C. | B能和浓溴水发生反应,1mol B最多消耗4molBr2 | |
| D. | C分子中含有手性碳原子. |
13.下列关于元素化合价的叙述中,错误的是( )
| A. | ⅢA族的B和Al都能形成+3价的化合物 | |
| B. | ⅤA族的N和P都能形成-3价的化合物 | |
| C. | ⅠA族的Na和K都能形成+1价的化合物 | |
| D. | ⅦA族的F和Cl都能形成+7价的化合物 |
20.实现下列变化时,需要克服相同类型作用力的是( )
| A. | 水晶和干冰的熔化 | B. | 食盐和醋酸钠的熔化 | ||
| C. | 乙醇和HCl溶于水 | D. | HCl和NaCl溶于水 |
17.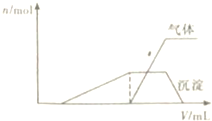 1L某混合溶液,可能含有的离子如表:
1L某混合溶液,可能含有的离子如表:
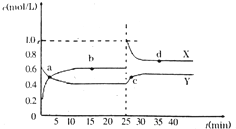
(1)往该溶液中逐滴加入NaOH溶液并适当加热,产生沉淀和气体的物质的量(n)与加入NaOH溶液的体积(V)的关系如图所示.
①则该溶液中一定不含有的离子是H+、NH4+、Al3+;
②可能存在的阳离子有K+;
③肯定不存在的阴离子是ClO-、AlO2-.
(2)经检测,该溶液中还含有大量的Cl-、Br-、I-,若向2L该混合溶液中通入一定量的Cl2,溶液中Cl-、Br-、I-的物质的量与通入Cl2的体积(标准状况)的关系如表所示,分析后回答下列问题.
①a的值为0.15;
②当通入Cl2的体积为3.36L(标准状态下)时,溶液中发生反应的离子方程式为Cl2+2I-=2Cl-+I2;此时溶液中Br-、I-的物质的量浓度分别为c(Br-)=0.75mol/L,c(I-)=0.05mol/L.
 1L某混合溶液,可能含有的离子如表:
1L某混合溶液,可能含有的离子如表:| 可能大量含有的阳离子 | H+、NH+、Al3+、K+ |
| 可能大量含有的阴离子 | Cl-、Br-、I-、ClO-、AlO2- |
①则该溶液中一定不含有的离子是H+、NH4+、Al3+;
②可能存在的阳离子有K+;
③肯定不存在的阴离子是ClO-、AlO2-.
(2)经检测,该溶液中还含有大量的Cl-、Br-、I-,若向2L该混合溶液中通入一定量的Cl2,溶液中Cl-、Br-、I-的物质的量与通入Cl2的体积(标准状况)的关系如表所示,分析后回答下列问题.
| Cl2的体积(标准状况) | 2.8L | 5.6L | 11.2L |
| n(Cl-) | 1.25mol | 1.5mol | 2mol |
| n(Br-) | 1.5mol | 1.4mol | 0.9mol |
| n(I-) | a mol | 0 | 0 |
②当通入Cl2的体积为3.36L(标准状态下)时,溶液中发生反应的离子方程式为Cl2+2I-=2Cl-+I2;此时溶液中Br-、I-的物质的量浓度分别为c(Br-)=0.75mol/L,c(I-)=0.05mol/L.