题目内容
9.若NA表示阿伏加德罗常数的值,下列叙述中正确的是( )| A. | 7.8gNa2O2所含离子总数为0.4NA | |
| B. | 2.0gD2O(重水)含有的质子数是NA | |
| C. | 标准状况下,0.5NA个HF分子所占的体积约为11.2L | |
| D. | 4℃时,18mL水分子中所含共价键的数目为4NA |
分析 A.过氧化钠含有的阴离子为过氧根离子;
B.质量转化为物质的量,结合1个水分子含有10个质子解答;
C.气体摩尔体积使用对象为气体;
D.4℃时,水的密度为1g/cm3,计算水的物质的量结合水分子结构计算共价键数.
解答 解:A.7.8gNa2O2物质的量为0.1mol,含0.2mol钠离子,0.1mol过氧根离子,含有离子总数为0.3NA,故A错误;
B.2.0gD2O(重水)的物质的量$\frac{2.0g}{20g/mol}$=0.1mol,含有质子数是0.1mol×10NA,即NA,故B正确;
C.标况下,HF为液体,不能使用气体摩尔体积,故C错误;
D.4℃时,水的密度为1g/cm3,18mL水的物质的量=$\frac{18g}{18g/mol}$=1mol,结合一个水分子结构中含有两个共价键可知共价键数2NA,故D错误;
故选B.
点评 本题考查了阿伏伽德罗常数的分析应用,主要是质量、物质的量计算微粒数,熟悉相关公式是解题关键,注意气体摩尔体积使用条件和对象,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
19.根据表中信息判断.下列选项正确的是( )
| 序号 | 反应物(均反应完全) | 生成物 |
| ① | Cl2、H2O2 | O2、… |
| ② | KMnO4,H2O2,H2SO4 | K2SO4、MnSO4… |
| ③ | Cl2、FeBr2 | FeCl3.FeBr3 |
| A. | ①反应中生成1molO2,转移4mole- | |
| B. | ②反应中的其余生成物只有H2O | |
| C. | ③反应中n(Cl2):n(FeBr2)=n(FeCl3):n(FeBr3)=1:2 | |
| D. | 由表知氧化性由强到弱顺序:MnO${\;}_{4}^{-}$>Cl2>H2O2>Fe2+>Br2 |
17.下列有关物质的用途说法不正确的是( )
| A. | 乙烯可作为部分水果或鲜花生长调节剂 | |
| B. | 乙炔燃烧时火焰温度高,氧炔焰可用于焊接或切割金属 | |
| C. | 甲醛的水溶液-福尔马林可用于杀菌、防腐 | |
| D. | 乙醇可用于萃取溴水中的溴单质 |
4.下列分子的空间构型为三角锥形的是( )
| A. | CO2 | B. | H2O | C. | NH3 | D. | H2 |
14.下列方法中不可以鉴别Fe3+和Fe2+的是( )
| A. | 通过物理方法观察他们颜色的区别 | |
| B. | 向两种溶液中加入NaOH溶液 | |
| C. | 向两种溶液中加入KSCN溶液 | |
| D. | 向两种溶液中加入氯水后再加入KSCN溶液 |
18.H、D、T、H+可以用来表示( )
| A. | 化学性质不同的氢原子 | B. | 四种不同的元素 | ||
| C. | 氢元素的四种不同粒子 | D. | 四种不同的氢元素 |
19.维生素C的结构简式如图: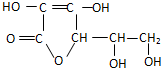 下列关于维生素C中所含官能团的说法错误的是( )
下列关于维生素C中所含官能团的说法错误的是( )
 下列关于维生素C中所含官能团的说法错误的是( )
下列关于维生素C中所含官能团的说法错误的是( )| A. | 含有羟基 | B. | 含有酯基 | C. | 含有碳碳双键 | D. | 含有醛基 |
 ,该元素的名称是氧;
,该元素的名称是氧; 用碱性锌锰电池做电源进行电解实验,装置如图.图中A装置中盛1L2mol/LAgNO3溶液,B装置盛1L2mol/LNa2SO4溶液,C和D为润湿的淀粉KI试纸的两端.通电后电解一段时间后,润湿的淀粉KI试纸的C端变蓝色.试回答:
用碱性锌锰电池做电源进行电解实验,装置如图.图中A装置中盛1L2mol/LAgNO3溶液,B装置盛1L2mol/LNa2SO4溶液,C和D为润湿的淀粉KI试纸的两端.通电后电解一段时间后,润湿的淀粉KI试纸的C端变蓝色.试回答: